
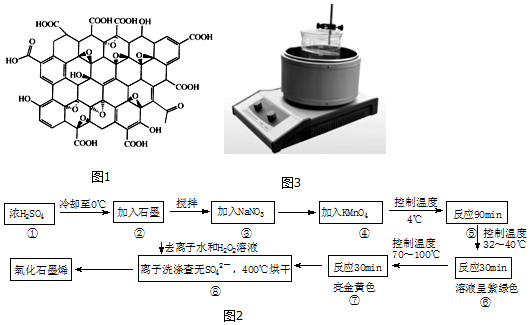
分析 (1)冰水混合物的温度是零度,据此回答;
(2)采用100目鳞片状的石墨可以增大石墨粒子表面积,提高氧化程度;图3示的“搅拌”方式为磁力搅拌;
(3)NaNO3和KMnO4中N、Mn元素的化合价较高,具有氧化性;
(4)高锰酸钾具有强的氧化性,酸性环境下可以将双氧水氧化,据此书写方程式;硫酸根离子可以和钡离子之间反应产生白色的沉淀,据此检验硫酸根离子.
解答 解:(1)冰水混合物的温度是零度,将浓硫酸“冷却至0℃”可采用的方法是用冰水浴,故答案为:用冰水浴;
(2)采用100目鳞片状的石墨,其主要目的是增大石墨粒子表面积,提高氧化程度,3示的“搅拌”方式为磁力搅拌;
故答案为:增大石墨粒子表面积,提高氧化程度;磁力搅拌;
(3)NaNO3和KMnO4中N、Mn元素的化合价较高,具有氧化性,骤③④中加NaNO3和KMnO4的作用就是利用的物质的氧化性.
故答案为:作氧化剂;
(4)高锰酸钾具有强的氧化性,酸性环境下可以将双氧水氧化,发生的反应为:2MnO4-+6H++5H2O2=5O2↑+2Mn2++8H2O,硫酸根离子可以和钡离子之间反应产生白色的沉淀,验洗涤已无SO42-的方法是:取少量最后一次的离心洗涤滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.故答案为:2MnO4-+6H++5H2O2=5O2↑+2Mn2++8H2O;取少量最后一次的离心洗涤滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
点评 本题以实验设计方案的考查方式来考查物质的性质以及实验技能,注意知识的迁移应用是关键,难度中等.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
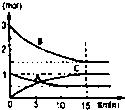 在某容积不变的密闭容器中,有可逆反应:mA(g)+nB(g)?pC(g)+qD(S)△H<0如图某反应过程中各物质物质的量n(mol)随时间t的变化曲线图.
在某容积不变的密闭容器中,有可逆反应:mA(g)+nB(g)?pC(g)+qD(S)△H<0如图某反应过程中各物质物质的量n(mol)随时间t的变化曲线图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1mol/L氯化钠溶液 | B. | 5 mL 2mol/L 氯化铵溶液 | ||
| C. | 150 mL 1mol/L氯化钾溶液 | D. | 75 mL 1.5mol/L 氯化镁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提高风能、太阳能等可再生清洁能源的使用比例 | |
| B. | 推广CO2再利用技术,将其合成有价值的化学品 | |
| C. | 利用工业废水灌溉农作物,提高水资源的利用率 | |
| D. | 研发煤炭的洁净、高效利用技术,保护生态环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 火炬燃料丙烷充分燃烧后只生成二氧化碳和水 | |
| B. | 撑杆跳高运动员使用的碳纤维撑杆属于有机高分子材料 | |
| C. | 泳池中加入的适量漂白粉可起到杀菌消毒作用 | |
| D. | 举重和体操运动员手上涂抹的碳酸镁白色粉末可吸水防滑 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com