

分析 原料A为盐酸,SiO2和盐酸不反应,氧化铝、氧化铁与盐酸反应,步骤①分离不溶固体与液体,为过滤操作,得到滤渣为SiO2,滤液1含有AlCl3、FeCl3及剩余的HCl,加入试剂B得到沉淀与滤液2,步骤②为过滤,步骤③通入的为二氧化碳,生成的沉淀为氢氧化铝,所以滤液②含有AlO2-,步骤②应加入氢氧化钠,将Fe3+转化为Fe(OH)3沉淀,将Al3+转化为AlO2-,氢氧化铝加入分解得到氧化铝.
解答 解:原料A为盐酸,SiO2和盐酸不反应,氧化铝、氧化铁与盐酸反应,步骤①分离不溶固体与液体,为过滤操作,得到滤渣为SiO2,滤液1含有AlCl3、FeCl3及剩余的HCl,加入试剂B得到沉淀与滤液2,步骤②为过滤,步骤③通入的为二氧化碳,生成的沉淀为氢氧化铝,所以滤液②含有AlO2-,步骤②应加入氢氧化钠,将Fe3+转化为Fe(OH)3沉淀,将Al3+转化为AlO2-,氢氧化铝加入分解得到氧化铝.
(1)步骤①加入盐酸,氧化铝与盐酸反应生成氯化铝与水,氧化铁与盐酸反应生成氯化铁与水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O,
故答案为:Al2O3+6H+=2Al3++3H2O;Fe2O3+6H+=2Fe3++3H2O;
(2)由上述分析可知,原料B的化学式是NaOH,步骤①加入过量盐酸,滤液①中含有Al3+、Fe3+、H+等,加入氢氧化钠,除去铁离子,将铝离子转化为AlO2-,反应离子方程为:H++OH-=H2O,Fe3++3OH-=Fe(OH)3↓,Al3++4OH-=AlO2-+2H2O.
故答案为:NaOH; H++OH-=H2O、Fe3++3OH-=Fe(OH)3、Al3++4OH-=AlO2-+2H2O;
(3)滤液②含有AlO2-,步骤③通入二氧化碳,与AlO2-反应生成的沉淀为氢氧化铝,反应进行方程式为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,
故答案为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3.
点评 本题以框图题形式考查化学工艺流程、物质的分离提纯、铝的化合物的性质,难度中等,是对知识迁移的综合运用.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 湿法 | 强碱介质中,Fe(NO3)3与NaClO反应得到紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸钾(K2FeO4)和KNO2等产物 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
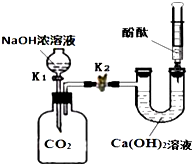 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.
某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和滴定实验中,盛装待测液的锥形瓶没有润洗,对实验结果无影响 | |
| B. | 用容量瓶配制一定物质的量浓度的溶液,定容时俯视刻度线,所配溶液浓度偏低 | |
| C. | 用润湿的pH试纸测某溶液的pH,测定结果不一定有误差 | |
| D. | 测定中和热的实验中,将碱液缓慢倒入酸溶液中,所测中和热值偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化反应、加成反应 | B. | 还原反应、氧化反应 | ||
| C. | 氧化反应、取代反应 | D. | 加成反应、水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com