
分析 (1)根据用酚酞作指示剂时,当滴进最后一滴溶液由红色变无色,且半分钟内不变色,则到达滴定终点;
(2)根据c(待测)=$\frac{V(标准)×c(标准)}{V(待测)}$分析不当操作对c(待测)的影响,以此判断浓度的误差;
(3)根据消耗盐酸的平均体积和物质的量浓度求出氢氧化钠的物质的量,再计算烧碱样品的纯度.
解答 解:(1)用酚酞作指示剂时,当滴进最后一滴溶液由红色变无色,且半分钟内不变色,则到达滴定终点;
故答案为:当滴进最后一滴溶液由红色变无色,且半分钟内不变色;
(2)若酸式滴定管没用标准盐酸润洗,标准液浓度降低,造成V(标)偏大,根据c(待测)=$\frac{V(标准)×c(标准)}{V(待测)}$分析可知c(待测)偏高;
故答案为:偏高;
(3)所耗盐酸标准液的体积分别为:(V2-V1)mL,依据
HCl~~~~~~NaOH
M mol/L×(V2-V1)×10-3L n(NaOH)
n(NaOH)=M(V2-V1)×10-3mol,
250mL的溶液中含有NaOH的质量为:M(V2-V1)×10-3mol×$\frac{250mL}{25mL}$×40g/mol,
烧碱样品的纯度为$\frac{M({V}_{2}-{V}_{1})×1{0}^{-3}mol×\frac{250mL}{25mL}×40g/mol}{Wg}$×100%=$\frac{40M({V}_{2}-{V}_{1})}{W}$%,
故答案为:$\frac{40M({V}_{2}-{V}_{1})}{W}$%.
点评 本题主要考查了酸碱中和滴定的操作、误差分析以及有关的化学计算,难度中等,掌握中和滴定的原理是解题的关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质编号 | 所属类别编号 | 物质编号 | 所属类别编号 |
| (1) | (3) | ||
| (2) | (4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y只能形成一种化合物 | |
| B. | 原子半径:r(Y)<r(W)<r(Z) | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | Z的最高价氧化物对应的水化物是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
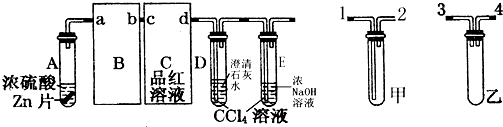
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
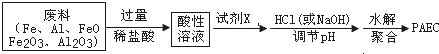
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子及其离子的核外电子层数等于该元素所在周期数 | |
| B. | 稀有气体元素原子的最外层电子数都是8 | |
| C. | 元素周期表从ⅢB到ⅡB 10个纵行的元素都是金属元素 | |
| D. | 短周期元素中,若两种元素的原子序数相差8,则它们的周期数一定相差1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com