

| A、该硫酸的物质的量浓度为9.2mol?L-1 |
| B、1 mol Zn与足量的该硫酸反应生成2g氢气 |
| C、该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2mol?L-1 |
| D、向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol |
| 1000ρω |
| M |
| 1000×1.84×98% |
| 98 |
| c1V1 |
| V2 |
| 18.4V1 |
| V2 |


科目:高中化学 来源: 题型:
| A、常温常压下,48gO3与O2混合气体中含氧原子数为3NA |
| B、1.8g的NH4+离子中含有的电子数为0.1NA |
| C、11.2L氧气中所含有的原子数为NA |
| D、标准状况下,22.4 LC6H14中所含碳原子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、摩尔可以把物质的宏观数量与微观粒子的数量联系起来 |
| C、摩尔是物质的量的单位,简称摩,符号为mol |
| D、国际上规定,0.012kg碳原子所含有的碳原子数目为1摩尔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能全部透过半透膜 |
| B、用激光笔照射有光亮的“通路” |
| C、所得溶液一定能导电 |
| D、所得物质一定为悬浊液或乳浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤⑦ | B、④⑤⑦ |
| C、③④⑥ | D、⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
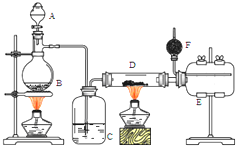 无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al+6HCl(g)═2AlCl3+3H2.完成下列填空:
无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾.实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al+6HCl(g)═2AlCl3+3H2.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:
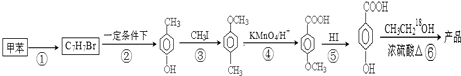
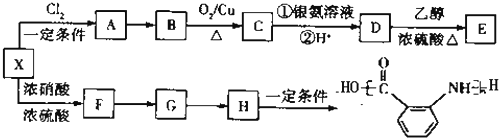
 在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式)
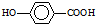
在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) 的同分异构体很多,其中符合下列条件有
的同分异构体很多,其中符合下列条件有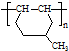 是一种建筑材料,根据题中合成路线信息,以甲苯为原料合成该高分子化合物,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:
是一种建筑材料,根据题中合成路线信息,以甲苯为原料合成该高分子化合物,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com