

分析 (1)黄铜矿与空气反应生成Cu和Fe的低价硫化物二氧化硫:产物为Cu2S、FeS、SO2;SO2能够被溴氧化为硫酸;聚硅酸铁净水是利用其吸附作用;
(2)Cu2S被氧化为Cu2O:2Cu2S+3O2 $\frac{\underline{\;高温\;}}{\;}$2Cu2O+2SO2;2Cu2O+Cu2S $\frac{\underline{\;高温\;}}{\;}$6Cu+2SO2↑,据含铜量相同计算;
(3)电解精炼铜时,粗铜作阳极,该电极上Zn、Fe、Ni、Cu失电子,精铜作阴极,该极上是铜离子得电子,阳极上铜以及比铜活泼的金属会溶解,而没有铜活泼的金属会从阳极掉落下,形成阳极泥.
解答 解:(1)黄铜矿与空气反应生成Cu2S、FeS、SO2,根据化合价升降相等配平,反应方程式为:2CuFeS2+O2 $\frac{\underline{\;高温\;}}{\;}$Cu2S+2FeS+SO2;SO2能够被溴氧化为硫酸,反应方程式为:SO2+Br2+2H2O=H2SO4+2HBr;聚硅酸铁净水是利用其吸附作用,铝离子和铁离子能够水解产生胶体,能够通过吸附净水,硫酸镁不具备该性质,
故答案为:2CuFeS2+O2$\frac{\underline{\;高温\;}}{\;}$ Cu2S+2FeS+SO2;SO2+Br2+2H2O=H2SO4+2HBr;b;
(2)Cu2S被氧化为Cu2O的反应方程式为:2Cu2S+3O2 $\frac{\underline{\;高温\;}}{\;}$2Cu2O+2SO2;Cu2O与Cu2S发生反应的方程式为:2Cu2O+Cu2S $\frac{\underline{\;高温\;}}{\;}$6Cu+2SO2↑,总方程式为:3Cu2S+3O2$\frac{\underline{\;高温\;}}{\;}$ 6Cu+3SO2,
含铜量相同时,设需要CuFeS2的质量为xt,则有40%xt×$\frac{M(Cu)}{M(CuFe{S}_{2})}$×100%=2t×98%,x=4.9t,
故答案为:3Cu2S+3O2$\frac{\underline{\;高温\;}}{\;}$ 6Cu+3SO2;4.9;
(3)a、电解池中,电能不会全部转化为化学能,还会伴随热能等形式的能的产生,故a错误;
b、电解精炼铜时,粗铜作阳极,接电源正极,发生氧化反应,故b正确;
c、溶液中Cu2+向阴极移动,在阴极上发生还原反应,故c错误;
d、在阳极上,没有铜活泼的金属Ag、Pt、Au等金属会从阳极掉落下,形成阳极泥,利用阳极泥可回收Ag、Pt、Au等金属,故d正确;
故答案为:bd.
点评 本题考查铜及其化合物的性质、电解精炼铜的工作原理,特别是考查了学生阅读信息、处理信息的能力,难度稍大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 无水四氯化锡(SnCl4)是一种用途广泛的锡化工中间体,纯品为无色液体,熔点-33℃,沸点114.1℃,易挥发,在湿空气中易水解而发烟.某同学设计用氯气与精锡反应制备无水四氯化锡,实验装置如图(部分夹持装置未画出):
无水四氯化锡(SnCl4)是一种用途广泛的锡化工中间体,纯品为无色液体,熔点-33℃,沸点114.1℃,易挥发,在湿空气中易水解而发烟.某同学设计用氯气与精锡反应制备无水四氯化锡,实验装置如图(部分夹持装置未画出):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
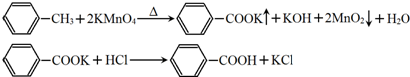
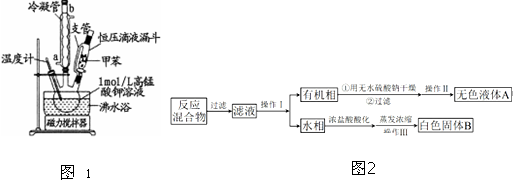
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体加入水中,加热溶解,冷却结晶、过滤. | 得到白色晶体和无色溶液 | ╲ |
| ② | 取少量滤液于试管中,滴入适量的硝酸酸化的AgNO3溶液. | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,加热使其熔化,测其熔点. | 白色晶体在122.4℃左右时完全熔化 | 白色晶体是苯甲酸 |
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
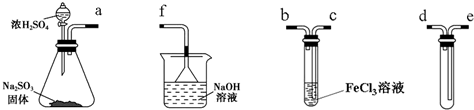
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.0 m o l/L | B. | 4.0 m o l/L | C. | 4.5 m o l/L | D. | 3.0 m o l/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铅蓄电池的A极为负极,电极材料为Pb | |
| B. | 铅蓄电池工作过程中每通过电路中2mol电子则消耗1molH2SO4 | |
| C. | 该电解池的阴极反应为 2NO3-+6H2O+10e-=N2↑+12OH- | |
| D. | 若电解过程中转移5moL电子,则交换膜两侧电解液的质量变化差(△m左-△m右)为14.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量溴水中 | B. | 分别在空气中燃烧 | ||
| C. | 通入酸性高锰酸钾溶液中 | D. | 在一定条件下通入氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com