
【题目】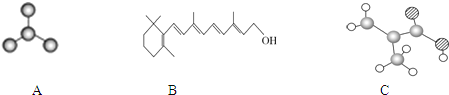
(1)图A是由4个碳原子结合成的某种烷烃(氢原子没有画出)。
①写出该有机物的系统命名法的名称_____________。
②该有机物的同分异构体的二氯取代物有_____________种。
(2)图B的键线式表示维生素A的分子结构。
①该分子的化学式为_____________。
②1mol维生素A最多可与_____________molH2发生加成反应。
(3)某物质只含C、H、O三种元素,其分子模型如图C所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
①该物质的结构简式为_____________。
②该物质中所含官能团的名称为_________________和_________________。
(4)下列实验操作不正确的是_________________
A.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液。
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验。
C.醇中含有少量水可加入硫酸铜再蒸馏制得无水乙醇
D.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,然后加热制取乙酸乙酯
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动。
F.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
【答案】 2-甲基丙烷 6 C21H32O5 5 CH2=C(CH)3COOH 碳碳双键 羧基 ACD
【解析】试题分析:(1)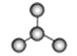 是含有4个碳原子的烷烃,结构简式是
是含有4个碳原子的烷烃,结构简式是![]() ;
;![]() 的同分异构体的结构简式是CH3CH2CH2CH3;(2)①根据图B的键线式书写维生素A的分子式;②发生加成反应时,1个碳碳双键消耗1个氢气分子;(3)根据C的分子模型
的同分异构体的结构简式是CH3CH2CH2CH3;(2)①根据图B的键线式书写维生素A的分子式;②发生加成反应时,1个碳碳双键消耗1个氢气分子;(3)根据C的分子模型 ,可知C的结构简式是
,可知C的结构简式是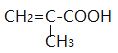 ;(4)验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,需要加入硝酸中和氢氧化钠;将铜丝弯成螺旋状,在酒精灯上加热变为氧化铜,热的氧化铜与无水乙醇反应,乙醇被氧化为乙醛;醇中含有少量水可加入生石灰再蒸馏制得无水乙醇;制取乙酸乙酯时,首先加入乙醇,然后再加入浓硫酸和乙酸,然后加热;加入碎瓷片可以防止液体爆沸;将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止,可以制得银氨溶液。
;(4)验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,需要加入硝酸中和氢氧化钠;将铜丝弯成螺旋状,在酒精灯上加热变为氧化铜,热的氧化铜与无水乙醇反应,乙醇被氧化为乙醛;醇中含有少量水可加入生石灰再蒸馏制得无水乙醇;制取乙酸乙酯时,首先加入乙醇,然后再加入浓硫酸和乙酸,然后加热;加入碎瓷片可以防止液体爆沸;将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止,可以制得银氨溶液。
解析:(1)① 是含有4个碳原子的烷烃,结构简式是
是含有4个碳原子的烷烃,结构简式是![]() ,系统命名是2-甲基丙烷;②
,系统命名是2-甲基丙烷;②![]() 的同分异构体的结构简式是CH3CH2CH2CH3,二氯取代物的结构简式是CHCl2CH2CH2CH3、CH2ClCHClCH2CH3、CH2ClCH2CHClCH3、CH2ClCH2CH2CH2Cl、CH3CCl2CH2CH3、CH3CHClCHClCH3,共6种。(2)①根据图B的键线式,维生素A的分子式是C21H32O5;②维生素A的分子中含有5个碳碳双键,所以1mol维生素A最多可与5molH2发生加成反应;(3)①根据C的分子模型
的同分异构体的结构简式是CH3CH2CH2CH3,二氯取代物的结构简式是CHCl2CH2CH2CH3、CH2ClCHClCH2CH3、CH2ClCH2CHClCH3、CH2ClCH2CH2CH2Cl、CH3CCl2CH2CH3、CH3CHClCHClCH3,共6种。(2)①根据图B的键线式,维生素A的分子式是C21H32O5;②维生素A的分子中含有5个碳碳双键,所以1mol维生素A最多可与5molH2发生加成反应;(3)①根据C的分子模型 ,可知C的结构简式是
,可知C的结构简式是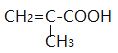 ;②
;②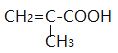 中所含官能团的名称为碳碳双键和羧基;(4)验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,需要加入硝酸中和氢氧化钠,再加入硝酸银,故A错误;将铜丝弯成螺旋状,在酒精灯上加热变为氧化铜,热的氧化铜将乙醇氧化为乙醛,故B正确;醇中含有少量水可加入生石灰再蒸馏制得无水乙醇;故C错误;制取乙酸乙酯时,首先加入乙醇,然后再加入浓硫酸和乙酸,然后加热,故D错误;加入碎瓷片可以防止液体爆沸,故E正确;将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止,得到银氨溶液,故F正确。
中所含官能团的名称为碳碳双键和羧基;(4)验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,需要加入硝酸中和氢氧化钠,再加入硝酸银,故A错误;将铜丝弯成螺旋状,在酒精灯上加热变为氧化铜,热的氧化铜将乙醇氧化为乙醛,故B正确;醇中含有少量水可加入生石灰再蒸馏制得无水乙醇;故C错误;制取乙酸乙酯时,首先加入乙醇,然后再加入浓硫酸和乙酸,然后加热,故D错误;加入碎瓷片可以防止液体爆沸,故E正确;将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止,得到银氨溶液,故F正确。


科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的脱氧剂,其制备方法是向Na2CO3溶液中通入SO2,生成NaHSO3和CO2,一定条件下NaHSO3转化为Na2S2O5。
完成下列填空:
(1)碳原子的原子结构示意图是____________。氧原子核外能量不同的电子有_____种。CO2的电子式是_________________。
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。______________________
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为_______________。
证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________。
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,氧化产物是_____;若反应中转移了0.04 mol的电子,有____g Na2S2O5参加反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与应用不相对应的是
A. Na2CO3的水溶液呈碱性,医学上能用作治疗胃酸过多
B. Na2O2能分别与H2O、 CO2反应,可用作供氧剂
C. 生石灰吸水能力强,常用作袋装食品的干燥剂
D. 铝是活泼的金属单质,铝可用于冶炼某些熔点较高的金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定Na2CO3和NaHCO3混合物样品的组成,称取不同质量样品溶于水后分别逐滴加入相同浓度盐酸30 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积)与加入样品的质量关系如图所示(不考虑CO2在水中的溶解、反应)。请计算:

(1)样品中n(Na2CO3) : n(NaHCO3)=____________。
(2)盐酸的物质的量浓度c(HCl)=________mol·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究溴乙烷的消去反应并验证产物。
实验原理:CH3CH2Br + NaOH![]() CH2=CH2↑ + NaBr + H2O
CH2=CH2↑ + NaBr + H2O
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。

(1)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因: 。
(2)丙同学认为只要对实验装置进行适当改进,就可避免对乙烯气体检验的干扰,改进方法为: 。
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(3)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是_______,此时发生反应的化学方程式为: 。
(4)结合资料二、三,有同学认为应将实验装置中烧瓶改成三颈烧瓶并增加两种仪器,这两种仪器是① 。② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+……,然后测定其质荷比。某有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )


A. 甲醇 B. 丙烷 C. 甲烷 D. 乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将7g某铜、银合金与足量的amol/LHNO3充分反应,完全溶解后放出的气体与标准状况下的氧气0.56L混合,通入水中恰好完全吸收,则此合金中银的质量是( )
A.1.6gB.2.7gC.3.2gD.5.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。已知鲨烯分子含30个C原子及6个碳碳双键且不含环状结构,则其分子式为( )
A.C30H60B.C30H56C.C30H52D.C30H50
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com