
【题目】如图所示的实验操作,不能达到相应目的是( )
A.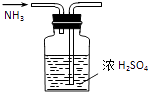 干燥NH3
干燥NH3
B.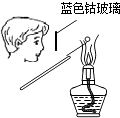 检验K2CO3中的K+
检验K2CO3中的K+
C.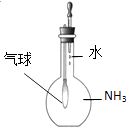 证明氨气极易溶于水
证明氨气极易溶于水
D.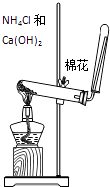 实验室制氨气
实验室制氨气
【答案】A
【解析】解:A.浓硫酸具有酸性,氨气属于碱性气体,二者反应生成铵盐,所以不能用浓硫酸干燥氨气,且导气管应该采用“长进短出”原则,故A错误; B.K元素的焰色反应必须透过蓝色钴玻璃观察,滤去黄光的干扰,K元素焰色反应呈紫色,故B正确;
C.氨气溶于水,可导致烧瓶内压强减小,外界大气压不变,则气球体积变大,从而证明氨气易溶于水,故C正确;
D.加热条件下,氯化铵和氢氧化钙反应生成氨气,氨气密度小于空气,且常温下和空气不反应,可以采用向下空气法收集,该装置符合条件,故D正确;
故选A.
A.浓硫酸具有酸性,氨气属于碱性气体,二者反应生成铵盐;
B.K元素的焰色反应必须透过蓝色钴玻璃观察;
C.氨气易溶于水,可导致烧瓶内压强减小;
D.加热条件下,氯化铵和氢氧化钙反应生成氨气,氨气密度小于空气,且常温下和空气不反应,可以采用向下空气法收集.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】一定条件下将0.1mol N2和0.3mol H2置于密闭容器中发生反应:N2+3H2 ![]() 2NH3 . 下列关于该反应的说法正确的是( )
2NH3 . 下列关于该反应的说法正确的是( )
A.最终可生成0.2 mol NH3
B.增大压强能使反应速率减小
C.降低反应体系的温度能加快反应速率
D.向容器中再加入N2 , 能加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
(1)X与Y所形成化合物晶体的晶胞如图所示.在1个晶胞中,X离子的数目为 .
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是 .
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 .
(4)Y与Z可形成YZ42﹣ , YZ42﹣的空间构型为(用文字描述);写出一种与YZ42﹣互为等电子体的分子的化学式: . 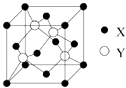
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是( )
A.炒菜时放入食盐并不破坏NaCl中的化学键
B.HCl的电子式是 ![]()
C.NaCl熔化时破坏共价键
D.HCl的结构式是H﹣Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有下列键型的物质,可能为单质的是
A. 只有离子键的物质 B. 既有离子键,又有非极性键的物质
C. 既有极性键,又有离子键的物质 D. 只有非极性键的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.氯碱工业中电解饱和食盐水:2Cl﹣+2H2O ![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
B.氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+
C.氢氧化钠溶液吸收少量二氧化硫SO2+OH﹣=HSO3﹣
D.稀硫酸中加氢氧化钡溶液至中性:Ba2++H++OH﹣+SO42﹣=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2O(g)=H2O(l)△H=﹣44kJ/mol,所以该过程是放热反应
B.人类利用的能源都是通过化学反应获得的
C.2CO(g)+O2 ![]() 2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量
2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量
D.需要加热的反应一定是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com