
【题目】某兴趣小组模拟工业制漂白粉,设计了如图所示的实验装置.已知:①氯气和碱反应放出热量.②6Cl2+6Ca(OH)2 ![]() 5CaCl2+Ca(ClO3)2+6H2O.
5CaCl2+Ca(ClO3)2+6H2O. 
回答下列问题:
(1)甲装置中仪器a的名称是 , MnO2在反应中所起的作用是 .
(2)装置乙中饱和食盐水的作用是 .
(3)①制取漂白粉的化学方程式是 . ②该小组制得的漂白粉中n(CaCl2) 远大于n[Ca(ClO)2],其主要原因是 .
③为提高Ca(ClO)2的含量,可采取的措施是(任写一种即可).
(4)漂白粉应密封保存,原因是(用化学方程式表示).
【答案】
(1)分液漏斗;作氧化剂
(2)除去氯气中混有的氯化氢
(3)2Cl2+2 Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;氯气和碱反应会放出热量,导致温度升高,发生了副反应:6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O;将丙装置浸在盛有冷水的水槽中或控制氯气产生速率
5CaCl2+Ca(ClO3)2+6H2O;将丙装置浸在盛有冷水的水槽中或控制氯气产生速率
(4)Ca(ClO)2+CO2+H2O=CaCO3+2HClO
【解析】解:(1)甲装置中仪器a具有球形特征,有玻璃活塞,在该实验中,可以控制加入的浓盐酸,为分液漏斗,装置A制取Cl2,反应的方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,反应中,MnO2中Mn元素化合价降低(+4→+2),MnO2为氧化剂,
MnCl2+Cl2↑+2H2O,反应中,MnO2中Mn元素化合价降低(+4→+2),MnO2为氧化剂,
所以答案是:分液漏斗;作氧化剂; (2)浓盐酸和二氧化锰反应过程中会发出氯化氢气体,氯化氢在氯化钠饱和溶液中易溶,而氯气难溶,通过饱和食盐水的作用是除去Cl2中混有的HCl气体,
所以答案是:除去氯气中混有的氯化氢;(3)①漂白粉的主要成分是次氯酸钙[Ca(ClO)2]和氯化钙,将氯气通入石灰乳[Ca(OH)2]制取漂白粉,同时有水生成,反应的化学方程式为:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,
所以答案是:2Cl2+2 Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
②氯气和碱反应会放出热量,导致温度升高,当温度低时,氯气和氢氧化钙反应生成氯化钙和次氯酸钙和水;当温度高时,发生了副反应:6Cl2+6Ca(OH)2 ![]() 5CaCl2+Ca(ClO3)2+6H2O,所以制得的漂白粉中n(CaCl2) 远大于n[Ca(ClO)2],
5CaCl2+Ca(ClO3)2+6H2O,所以制得的漂白粉中n(CaCl2) 远大于n[Ca(ClO)2],
所以答案是:氯气和碱反应会放出热量,导致温度升高,发生了副反应:6Cl2+6Ca(OH)2 ![]() 5CaCl2+Ca(ClO3)2+6H2O;
5CaCl2+Ca(ClO3)2+6H2O;
③温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,用冰水或冷水冷却,或控制氯气产生速率,通过控制反应速率,避免反应放热瞬时升高,
所以答案是:将丙装置浸在盛有冷水的水槽中或控制氯气产生速率;(4)漂白粉有效成分为次氯酸钙,HClO虽是强氧化性的酸,但它是比碳酸还弱的酸,受空气中的水、CO2作用而导致变质,生成CaCO3和HClO,该反应的化学方程式为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,所以漂白粉应密封保存,
所以答案是:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO.


科目:高中化学 来源: 题型:
【题目】某烃的结构简式如图,下列说法不正确的是( ) 
A.1mol该烃完全燃烧消耗O211mol
B.与氢气完全加成后的产物中含2个甲基
C.1mol该烃完全加成消耗Br23mol
D.分子中一定共平面的碳原子有6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1﹣丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反 应装置如图.下列对该实验的描述错误的是( )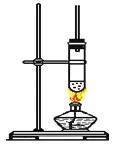
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.浓硫酸的作用是催化剂和吸水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,国际原油价格大幅上涨,促使各国政府加大生物能源生产,其中乙醇汽油已进入实用化阶段.
(1)乙醇官能团的电子式为;
(2)乙醇在铜或银做催化剂的条件下,可以被空气中的氧气氧化成X,该反应的化学方程式是;
(3)乙醇可以被直接氧化成Y(Mr=60),需要加入的试剂是;在浓硫酸作用下,乙醇与Y反应可生成一种有香味的物质W,该反应的类型为;
(4)现有两瓶无色液体,分别盛有Y、W,只用一种试剂就可以鉴别,该试剂可以是
A.水
B.乙醇
C.紫色石蕊试液
D.苯
E.碳酸钠溶液
(5)工业上通过乙烯与水在一定条件下反应制得乙醇,反应类型是 , 现代石油化工采用银做催化剂,乙烯能被氧气氧化生成M.;
(6)乙醇﹣氧气燃料电池是以KOH溶液作为电解质溶液,写出其负极的电极反应式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 在多电子的原子里,能量高的电子通常在离核近的区域内运动
B. 凡单原子形成的稳定离子,一定具有稀有气体元素原子的核外电子排布
C. 氯化氢属于共价化合物,溶于水能电离出H+、Cl—
D. 阴、阳离子通过静电引力而形成的化学键叫离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种有机物中:
A. B.CH3CH2CH2CH2CH3 C.CH3CH=CHCH3 D.CH3CH=CH2
B.CH3CH2CH2CH2CH3 C.CH3CH=CHCH3 D.CH3CH=CH2
(1)属于烷烃的是 (填序号,下同),互为同分异构体的是 ,互为同系物的是 .
(2)用系统命名法给A命名,其名称是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应N2O4(g)2NO2(g)△H=+57kJmol﹣1 , 在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( ) 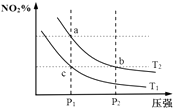
A.反应温度:T1>T2
B.b、c两点的反应速率:v(b)>v(c)
C.a、c两点气体的颜色:a浅,c深
D.a、b两点的平衡常数:Kb>Ka
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com