
 ×n��Na2S2O3��=
×n��Na2S2O3��= cb×10-3mol��
cb×10-3mol�� cb×10-3mol×127g/mol=
cb×10-3mol×127g/mol=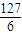 cb×10-3g��
cb×10-3g��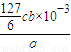 =
=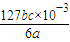 ���ʴ�Ϊ��
���ʴ�Ϊ��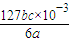 ��
�� ��
��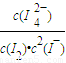 ��������ͬʱ��I3-���ӵ����ʵ����������ʼ��ռ�������ƣ���I-����Ũ�ȵ����ӣ�I3-���ӵ����ʵ����������ͣ�I42-���ӵ����ʵ����������ӣ�
��������ͬʱ��I3-���ӵ����ʵ����������ʼ��ռ�������ƣ���I-����Ũ�ȵ����ӣ�I3-���ӵ����ʵ����������ͣ�I42-���ӵ����ʵ����������ӣ�

 ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д� �㽭֮��ѧҵˮƽ����ϵ�д�
�㽭֮��ѧҵˮƽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 127bc��10-3 |
| 6a |
| 127bc��10-3 |
| 6a |
c
| ||
| c(I2)?c2(I-) |
c
| ||
| c(I2)?c2(I-) |
| KI��ʼŨ��/mol?L-1 | 0.02 | 0.04 | 0.06 | 0.08 | 0.10 |
| I3-% | 88.98 | 88.04 | 85.28 | 82.26 | 79.23 |
| I42-% | 4.38 | 8.67 | 12.60 | 16.21 | 19.53 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
126 53 |
127 53 |
128 53 |
131 53 |

- 3 |
- 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
| KI��ʼŨ��/mol?L-1 | 0.02 | 0.04 | 0.06 | 0.08 | 0.10 |
| I3-% | 88.98 | 88.04 | 85.28 | 82.26 | 79.23 |
| I42-% | 4.38 | 8.67 | 12.60 | 16.21 | 19.53 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ģ���� ���ͣ������


�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com