
【题目】以下变化是化学变化的是( )
A.升华B.潮解C.风化D.萃取
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】2016年8月5日在巴西里约召开的第31届奥运会,由于兴奋剂事件而使多名俄罗斯运动员遭到禁赛,禁止运动员使用兴奋剂是奥运会公平、公正的重要举措之一.以下有两种兴奋剂的结构分别为: 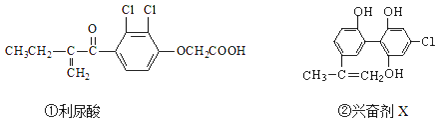
则关于以上两种兴奋剂的说法中不正确的是( )
A.利尿酸能发生取代反应、加成反应和酯化反应
B.1mol兴奋剂X与足量浓溴水反应,最多消耗3molBr2
C.可用FeCl3溶液检测利尿酸中是否含有兴奋剂X
D.1mol兴奋剂X最多都能和5molNaOH的溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质不能按![]() “
“![]() ” 表示反应一步完成关系转化的是
” 表示反应一步完成关系转化的是 ![]()
选项 | a | b | c |
A | SiO2 | Na2SiO3 | H2SiO3 |
B | AlCl3 | Al(OH)3 | NaAlO2 |
C | Fe | Fe(OH)3 | Fe2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物之间的相互转化可用下式表示:![]()
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4 . 若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是 (选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为﹣2价)则下列说法正确的是 (选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式: FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3 . 高铁酸钾作为水处理剂发挥的作用是 、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,相同质量的下列气体,占有体积由大到小的顺序是① Cl2② H2③ N2④ CO2⑤ O2
A.③②④⑤①B.⑤②④③①
C.①④⑤②③D.②③⑤④①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关 ![]() 分子结构的下列叙述中正确的是( )
分子结构的下列叙述中正确的是( )
①除苯环外的其余碳原子有可能都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上.
A.①②
B.②③
C.①③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应2A(g)+B(g) ![]() 2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
①用物质A表示反应的平均速率为0.3 mol/(L·s)
②用物质B表示反应的平均速率为0.6 mol/(L·s)
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol/L
其中正确的是( )
A.①③
B.①④
C.②③
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1:4
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某钠盐溶液中通入足量氨气,无明显现象.再在所得溶液中通入过量CO2 , 产生大量白色沉淀。
(1)写出氨气的电子式。
(2)该钠盐溶液中一定不可能含有下列哪种微粒(填编号)。
A.Cl﹣
B.Fe2+
C.SiO32﹣
D.AlO2﹣
(3)写出一个通入过量CO2时生成白色沉淀的离子方程式。
(4)Ⅱ.电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放.某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下: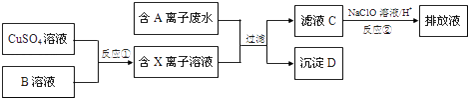
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,反应后的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
沉淀D的化学式是。
(5)写出沉淀D在氧气中灼烧发生的化学方程式。
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理。
(7)反应①为制得某种元素的低价X离子,从氧化还原反应的角度分析,(填“能”或“不能”用Na2SO3溶液来代替B溶液,原因是。
(8)设计实验证明所用Na2SO3溶液是否变质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com