
����Ŀ�����ͼ����������⡣
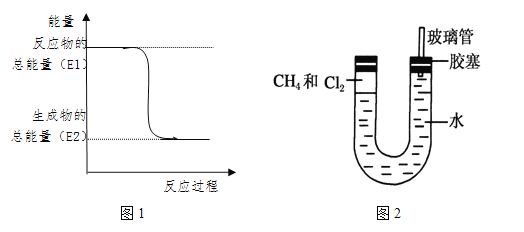
��1�����������䡱�еġ�����ָ��Ȼ��������Ҫ�ɷֵĽṹʽ��__________��һ�����ĸ�����ȼ�չ��̵������仯��ͼ1��ʾ����ͼ�п��Զ���E1 E2����������������÷�Ӧ_______ ����ų��������ա���������
��2��CH4��Cl2������һϵ�з�Ӧ����________(�Ӧ����)��Ӧ����д��CH4��Cl2��Ӧ����һ�ȼ���Ļ�ѧ����ʽ��_______________________________��
��3��������м���������Ļ�������װ�÷������й����ĵط����û�����建���ط�Ӧһ��ʱ�䡣��������Сʱ�ķ�Ӧ��ͼ2��U���Ҷ˵IJ�������ˮ���ı仯�� ������������½�������
���𰸡���1�� 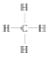 , E1��E2 ���ų�
, E1��E2 ���ų�
��2��ȡ����CH4+Cl2��CH3Cl+HCl��2�֣� ��3���½���2�֣�
��������
�����������1����Ȼ������Ҫ�ɷ�Ϊ���飬�ṹʽ�� ����ͼ��֪��Ӧ���������E1>�������������E2���÷�Ӧ�ų�������
����ͼ��֪��Ӧ���������E1>�������������E2���÷�Ӧ�ų�������
��2��CH4��Cl2������һϵ�з�Ӧ����ȡ����Ӧ��CH4��Cl2�ڹ�����������Ӧ����һ�ȼ������Ȼ��⣬��ѧ����ʽΪCH4+Cl2��CH3Cl+HCl��
��3��������������Ӧ���ɶ��ȼ��顢���ȼ�������Ȼ�̼������ΪҺ�壬���ɵ��Ȼ��⼫������ˮ�����U�ι����Һ���Ϸ���ѹ���ͣ�ˮ�����������Ҷ˵IJ�������ˮ���ı仯���½���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��mA(g)��nB(g) ![]() pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С����
pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С����
��1���÷�Ӧ���淴ӦΪ________�ȷ�Ӧ����m��n______p (�����������������) ��
��2����ѹʱ��A����������__________��(���������С�����䡱����ͬ)
��3�����ݻ��������B����B��ת����__________��
��4���������¶ȣ���ƽ��ʱB��C��Ũ��֮�Ƚ�__________��
��5�������������ƽ��ʱ��������������ʵ���__________��
��6����B����ɫ���ʣ�A��C����ɫ�������C(�������)ʱ�������ɫ__________����ά��������ѹǿ���䣬��������ʱ���������ɫ ��(����������dz�����䡱)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
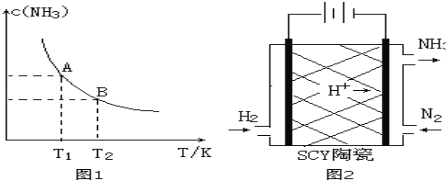
����Ŀ����1����һ�������£���1.00molN2��g����3.00molH2��g�������һ��10.0L�ܱ������У��ڲ�ͬ�¶��´ﵽƽ��ʱNH3��g����ƽ��Ũ����ͼ1��ʾ�������¶�ΪT1ʱƽ���������а������������Ϊ25.0%��
�����¶���T1�仯��T2ʱ��ƽ�ⳣ����ϵK1 K2�����������������=�������ʱ���H 0���������������
���÷�Ӧ��T1�¶���5.00min�ﵽƽ�⣬���ʱ����N2�Ļ�ѧ��Ӧ����Ϊ ��
��T1�¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K1= ��
��2���������¡��˹��̵������о��������ڳ��³�ѹ����������N2�ڴ���������ˮ������Ӧ��2N2��g��+6H2O��l��=4NH3��g��+3O2��g�����˷�Ӧ����S 0�������������������֪��N2��g��+3H2��g��=2NH3��g����H=a kJ/mol 2H2��g��+O2��g��=2H2O��l����H=b kJ/mol 2N2��g��+6H2O��l��=4NH3��g��+3O2��g������H= ���ú�a��b��ʽ�ӱ�ʾ����
��3����ѧ�Ҳ������Ӹߵ����Ե�SCY�մɣ��ɴ���H+��ʵ���˵��³�ѹ�¸�ת���ʵĵ绯ѧ�ϳɰ�����ʵ��ԭ��ʾ��ͼ��ͼ2��ʾ���������ĵ缫��Ӧʽ�� ��
��4����֪ijЩ���������ˮ�еĵ���ƽ�ⳣ����25�������±���
������� | H2CO3 | NH3.H2O |
����ƽ�ⳣ�� | Ka1=4.30��10-7 Ka2=5.61��10-11 | Kb=1.77��10-5 |
���г�����0��1 mol��L-1�ģ�NH4��2CO3��Һ��
������Һ�� �ԣ���ᡱ�����С����������ԭ���� ��
���ã�NH4��2CO3��Һ�и���Ũ��֮��Ĺ�ϵʽ����ȷ���� ��
A��c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3.H2O)
B��c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C��c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol/L
D��c(NH4+)+c(NH3.H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
E��c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)+c(NH3.H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���л���A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ������AΪ��Ҫԭ�Ϻϳ�������������ϳ�·������ͼ��ʾ��

��1��A�����й����ŵ������� ��D�й����ŵ�������________��Ӧ�ٵķ�Ӧ������ ��Ӧ��
��2����Ӧ���Ļ�ѧ����ʽ�� ��
��Ӧ���Ļ�ѧ����ʽ�� ��
��3��E�dz����ĸ߷��Ӳ��ϣ��ϳ�E�Ļ�ѧ����ʽ�� ��
��4��ijͬѧ����ͼ��ʾ��ʵ��װ����ȡ��������������ʵ��������Թܼ����ϲ�Ϊ���ġ�������ˮ����״Һ�塣

�� ʵ�鿪ʼʱ���Թܼ��еĵ��ܲ�����Һ���µ�ԭ���� ��
������ʵ���б���̼������Һ��������(����ĸ) ��
A���к�������Ҵ�
B���к����Ტ���ղ����Ҵ�
C�����������ڱ���̼������Һ�е��ܽ�ȱ���ˮ�и�С�������ڷֲ�����
D�������������ɣ���������
����ʵ��������B��D�Ʊ�����������ʵ���У�����1mol B��1mol D��ַ�Ӧ��__________����/���ܣ�����1mol ����������ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ���Ը÷�Ӧ���ƶϺ�������

A���÷�Ӧ�Ļ�ѧ����ʽΪ3B+2D 6A+4C
B����Ӧ���е�1 sʱ��v��A����3v��D��
C����Ӧ���е�6 sʱ��B��ƽ����Ӧ����Ϊ0.1mol/(Ls)
D����Ӧ���е�6 sʱ�������ʵķ�Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣����û�ѧ����ش�

��1������������Ӧ��ˮ������������ǿ���� ��
��2��ʵ������ȡ�����⻯��Ļ�ѧ����ʽ ��
��3��������Ԫ������������Ӧ��ˮ�������Ӧ�Ļ�ѧ����ʽ ��
��4��Ԫ������������Ԫ���γɵ�һ�ֻ����ﺬ�еĻ�ѧ�������� �������ʽΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
������� | �� | �� | �� | ������ | �⻯�� |
��ѧʽ | HCl ��________ | ��________ ��Ba(OH)2 | ��Na2CO3 ��______ | ��CO2 ��Na2O | ��NH3 ��H2O2 |
(1)��Na��K��H��O��C��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������ϱ����ڢۢ��ĺ��档
(2)д��ʵ���������Ʊ�O2�Ļ�ѧ����ʽ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ�飨ͼ��a��b��c��ʾֹˮ�У���
![]()
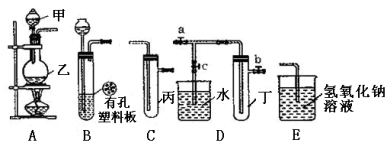
��1���ס����������������� ��
��2��A��C��E�������װ�ÿ�������ȡCl2��д��A�з�����Ӧ�Ļ�ѧ����ʽ ����Cl2ͨ�뺬�з�̪��NaOH��Һ�е������� ���÷�Ӧ�����ӷ���ʽΪ ��
��3��B��D��Eװ����������B��ʢװŨ�����ͭƬ��ͭƬ�����п����ϰ��ϣ������Ƶ�NO2�������й�ʵ�顣
��д���÷�Ӧ�����ӷ���ʽ ��
������Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ�� ���ٴ�ֹˮ�� ��ʹ�ձ��е�ˮ�����Թܶ��С�
���Թܶ��е�NO2��ˮ��ַ�Ӧ�������Թ��ڻ���ͨ��һ������O2��ֱ���Թ�ȫ������ˮ����������Һ�����ʵ����ʵ���Ũ���� mol��L1������2λ��Ч��ֵ�����尴��״�����㣩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������з�Ӧ�����������Dz��ܷ�������( )
A������ B������ C���ӳ� D��ˮ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com