
| A. | 元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| B. | 最外层电子数相同的元素一定属于同一族 | |
| C. | 非金属元素的最外层电子数都大于或等于4 | |
| D. | 同周期元素的电子层数相同 |
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:实验题
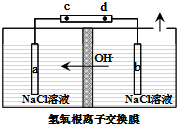 氯元素可以形成HClO、HClO2、HClO3、HClO4多种含氧酸.
氯元素可以形成HClO、HClO2、HClO3、HClO4多种含氧酸.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
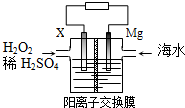
| A. | X可为铁、铜、石墨等电极 | |
| B. | 每转移2 mol电子,2mol H+由交换膜左侧向右侧迁移 | |
| C. | 正极的电极反应式为H2O2+2e-+2H+═2H2O | |
| D. | 该电池能将化学能全部转化成电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水结成冰体积膨胀,密度变小 | |
| B. | 31g白磷分子中存在的共价键数目是1.5NA(P的相对原子质量31) | |
| C. | DNA中的碱基互补配对是通过氢键来实现的 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
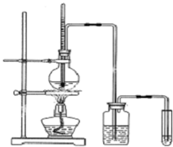 如图是实验室制乙烯并检验其性质的装置图,请回答:
如图是实验室制乙烯并检验其性质的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
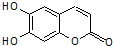 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A. | 2 mol Br2 2 mol NaOH | B. | 2 mol Br2 3 mol NaOH | ||
| C. | 3 mol Br2 4 mol NaOH | D. | 4 mol Br2 4 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和一氯甲烷 | B. | 淀粉和纤维素 | C. | 苯和甲苯 | D. | 蔗糖和麦芽糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com