下列叙述正确的是( )
A.浓度均为0.1mol?L-1的CH3COOH和CH3COONa溶液等体积混合所得的溶液中:c(CH3COOH)+c(CH3COO-)=0.2mol?L-1
B.0.1mol?L-1NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2(CO32-)
C.0.2mol?L-1HCl溶液与等体积0.1mol?L-1NaOH溶液混合后,溶液的pH=1
D.0.1mol?L-1氨水中滴入0.1mol?L-1盐酸至溶液呈中性时,混合溶液中:c(NH4+)=c(Cl-)
【答案】
分析:A.溶液稀释前后溶质的物质的量不变,但浓度减小;
B.从物料守恒的角度分析;
C.计算反应后的溶液的c(H
+),可计算pH;
D.从电荷守恒的角度分析.
解答:解:A.物质的量浓度各为0.1mol?L
-1的CH
3COOH和CH
3COONa溶液等体积混合后,溶液为原来的体积的2倍,则有:c(CH
3COOH)+c(CH
3COO
-)=0.1mol/L,故A错误;
B.根据物料守恒可知,溶液中应存在c(Na
+)=c(HCO
3-)+c(H
2CO
3)+(CO
32-),故B错误;
C.c(H
+)=
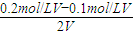
=0.05mol/L,则pH=1.7,故C错误;
D.反应后的溶液电荷守恒,存在c(NH
4+)+c(H
+)=c(Cl
-)+c(OH
-),溶液呈中性,则有c(H
+)=c(OH
-),所以有c(NH
4+)=c(Cl
-),故D正确.
故选D.
点评:本题综合考查离子浓度的大小比较,题目难度中等,本题注意从物料守恒和电荷守恒的角度分析,注意A项,为易错点,不要忽视浓度的变化.

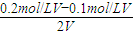 =0.05mol/L,则pH=1.7,故C错误;
=0.05mol/L,则pH=1.7,故C错误;
