
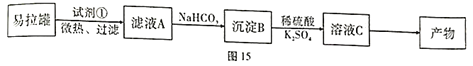
����Ŀ��KAl(SO4)2��12H2O(����)��һ�ָ��Σ�Ӧ�ù㷺�����÷�������(��Ҫ�ɷ�ΪAl������������Fe��Mg����)�Ʊ������Ĺ�����ͼ15��ʾ����ش��������⣺
��1����д��Al3+�Ľṹʾ��ͼ��______________________��
��2���Լ������ѡ��___________(�����)��д��A�ܽ�Ļ�ѧ����ʽ��_________________________��
A��HCl��Һ B��H2SO4��Һ C��NaOH��Һ D����ˮ
��3��д����ҺA������B�����ӷ���ʽ��______________________�������£�Al(OH)3![]() AlO2-+H++H2O K=2.0��10-13,H2CO3��Ka1=1��10-7��Ka2=4��10-11,������ҺA������B��ƽ�ⳣ�� K=___________��
AlO2-+H++H2O K=2.0��10-13,H2CO3��Ka1=1��10-7��Ka2=4��10-11,������ҺA������B��ƽ�ⳣ�� K=___________��
��4��д������ҺC�õ�����IJ�����__________________________________��
��5�������£�pHֵ��ȵ�NaAlO2��NaOH������Һ�У���ˮ�������c(OH-)ǰ��Ϊ���ߵ�108������������Һ��pH=___________��
���𰸡�![]() C2Al+2NaOH+2H2O=2NaAlO2+3H2��AlO2-+HCO3-+H2O=Al(OH)3��+CO32-200����Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ�����11
C2Al+2NaOH+2H2O=2NaAlO2+3H2��AlO2-+HCO3-+H2O=Al(OH)3��+CO32-200����Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ�����11
��������
���Ʊ����̿���֪��������������Ҫ�ɷ�Ϊ��Ҫ�ɷ�ΪAl������������Fe��Mg���ʣ��Լ���ΪNaOH��Fe��Mg����Ӧ��ֻ����2Al+2NaOH+2H2O=2NaAlO2+3H2�������˺�����Һ��NaAlO2����̼���ⰱ��Ӧ������������������BΪAl(OH)3���������ᡢ����صõ��������Դ��������
��1��Al3+�� �� �� �� Ϊ13�����������Ϊ10���ṹʾ��ͼΪ��![]() ��
��
��ˣ�������ȷ������![]() ��
��
(2) Fe��Mg��ǿ���Ӧ����Al��NaOH��Һ��Ӧ����Ϊ�����������������Լ���Ӧѡ��NaOH���������ܽ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2����
��ˣ�������ȷ������C��2Al+2NaOH+2H2O=2NaAlO2+3H2����
(3)��������������֪��������BΪAl(OH)3��̼�������������ǿ��ƫ����������ҺA������B�����ӷ���ʽ��AlO2-+HCO3-+H2O=Al(OH)3��+CO32-��ƽ�ⳣ�� K=![]() =
=![]() =
=![]() =
=![]() =200��
=200��
��ˣ�������ȷ������200��
��4������ҺC�õ������IJ���������Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ����
��ˣ�������ȷ����������Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ����
(5)NaAlO2��Һ��ˮ�ĵ����ܵ��ٽ�����NaOH��Һ��ˮ�ĵ����ܵ����ơ���������Һ��pH��a��NaAlO2��Һ��ˮ�������c(OH��)Ϊ10a��14mol��L��1��NaOH��Һ��ˮ�������c(OH��)Ϊ10��amol��L��1����10a-14��108��10-a����a��11��
��ˣ�������ȷ������11��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaClO2��һ����Ҫ��ɱ����������Ҳ������Ư��֯��ȣ���һ�������������£�

�ش��������⣺
��1��NaClO2��Cl�Ļ��ϼ�Ϊ_______��
��2��д������Ӧ������������ClO2�Ļ�ѧ����ʽ__________________________________��
��3������⡱����ʳ��ˮ�ɴ���ˮ���ƶ��ɣ�����ʱ��Ϊ��ȥMg2+��Ca2+��Ҫ������Լ��ֱ�Ϊ________��________������⡱��������Ӧ����Ҫ������______��
��4����β�����ա������ա���⡱�����ų�������ClO2�������շ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ________���÷�Ӧ������������_________��
��5������Ч�Ⱥ��������������������������������������䶨���ǣ�ÿ�˺��������������������൱�ڶ��ٿ�Cl2������������NaClO2����Ч�Ⱥ���Ϊ____����������������λС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������40�����ӣ���ȼ��ʱ���ɵ������CO2��H2O(g)�����л���ķ���ʽΪ (����)
A.C4H8
B.C4H10
C.C5H10
D.C5H12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��װ�ý��е���Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���( )
A. 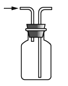 �ռ� NOB.
�ռ� NOB.  �Ʊ� NH3
�Ʊ� NH3
C.  �Ʊ� Fe(OH)2D.
�Ʊ� Fe(OH)2D. 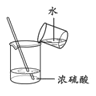 ϡ��Ũ H2SO4
ϡ��Ũ H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������;��Ӧ�и����ֵ������ǣ�
A��ǿ���� B���ӷ��� C����ˮ�� D����ˮ�� E��ǿ������ F�����ȶ���
��1�������м���Ũ���ᣬ���ñ�Ϊ��ɫ��ĩ__________��
��2�������۳�װ��Ũ�����Ũ����___________��
��3��Ũ���᳨�ڷ��û���������___________��
��4��Ũ������û���____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��NH3���ܽ��ԣ�ij��ȤС�鰴��ͼ��ʾװ�ý���ʵ�飨fΪֹˮ�У�����ش��������⣺
��1��д��ʵ�����ù��������װ����ȡ�����Ļ�ѧ����ʽ __________��
��2��Ҫ�õ�����İ�����ѡ��____���������
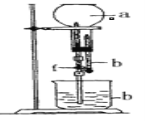
A����ʯ�ң�CaO��NaOH�Ļ���
B��Ũ����
C��Ũ����
D������������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����11�֣�
����ͼʾ�ش��������⣺
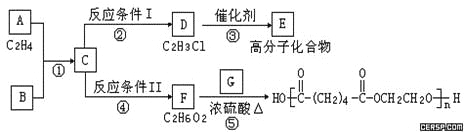
��1��д��A��E��G�Ľṹ��ʽ��A ��E ��G ��
��2����Ӧ���Ļ�ѧ����ʽ��������Ӧ�������� ����Ӧ����ѧ����ʽ��������Ӧ�������� ��
��3��д���������ķ�Ӧ���ͣ��� ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(NAΪ�����ӵ�����)(����)
A. 12 gʯī�к���C��C���ĸ���Ϊ1.5 NA
B. 12 g���ʯ�к���C��C���ĸ���Ϊ4 NA
C. 60 g SiO2�к���Si��O���ĸ���Ϊ2 NA
D. 124 g P4�к���P��P���ĸ���Ϊ4 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�������1mol��NH4Al(SO4)2��H2SO4���ϡ��Һ����μ���һ����Ba(OH)2��Һ������������������Ba(OH)2 �������ı仯��ͼ��ʾ���������ӷ���ʽ��д��ȷ����

A. O��A��H++SO42��+Ba2++OH����BaSO4��+H2O
B. A��B��2Al3++3SO42��+3Ba2+ +6OH����3BaSO4��+2Al(OH)3��
C. B��C��NH4++SO42��+Ba2+ +OH����BaSO4��+NH3��H2O
D. D��E��NH4++ OH����NH3��H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com