
【题目】下列反应不属于可逆反应的是( )
A.工业上利用氮气和氢气合成氨气
B.![]() 和
和![]()
C.密闭容器中的二氧化氮和四氧化二氮在一定压强下可以相互转化
D.密闭容器中的二氧化硫和氧气在一定条件下可以生成三氧化硫,同时三氧化硫又可以分解为二氧化硫和氧气
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】含手性碳原子的分子称手性分子,手性分子具有光学活性。如下图有机物具有光学活性(式中标有*号的为手性碳原子),也能发生下列反应,请问发生哪种反应后,该有机物仍然一定具有光学活性( )
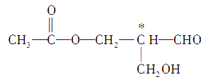
A. 消去反应 B. 水解反应 C. 银镜反应 D. 酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A. HA是强酸
B. 该混合液pH=7
C. 图中x表示HA,Y表示OH-,Z表示H+
D. 该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家设计出-套利用SO2和太阳能综合制氢方案,其基本工作原理如图所示,下列说法错误的是( )
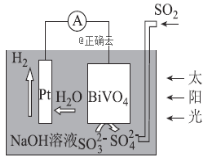
A.该电化学装置中,Pt电极作正极
B.BiVO4电极上的反应式为![]()
C.电子流向:Pt电极→导线→BiVO4电极→电解质溶液→Pt电极
D.OH-移向BiVO4电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为____。
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是___;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要如图中的____(填字母代号)。
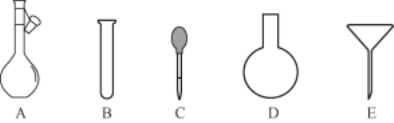
(3)滴定终点的判定现象是____。
(4)滴定分析时,称取TiO2(摩尔质量为M g/mol)试样w g,消耗c mol/LNH4Fe(SO4)2 标准溶液V mL,则TiO2质量分数表达式为____。
(5)下列操作对TiO2质量分数测定结果偏高的是(______)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出
②若在滴定终点读取滴定管刻度时,俯视标准液液面
③若在滴定时滴定前尖嘴部分有气泡,滴定后无气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温下的密闭容器中,有可逆反应![]() ,下列不能说明该反应已达到平衡状态的是( )
,下列不能说明该反应已达到平衡状态的是( )
A.正反应生成NO2的速率和逆反应生成O2的速率
B.混合气体的颜色不再改变
C.反应容器中的压强不随时间的变化而变化
D.混合气体的平均摩尔质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知293K时下列物质的溶度积![]() 单位已省略
单位已省略![]() :
:
| Ag2SO4 | FeS | CuS | Ag2S |
| 1.2×10-5 | 6.3×10-18 | 8.5×10-45 | 6.3×10-50 |
下列说法正确的是![]()
![]()
A.相同温度下,Ag2SO4、FeS、CuS饱和溶液中:![]()
B.向FeS悬浊液中滴加CuSO4溶液发生反应的离子方程式:![]()
C.浓度均为0.004mol/L的AgNO3和H2SO4溶液等体积混合后不能产生沉淀
D.向饱和Ag2S溶液中加少量Na2S固体,溶液中c(Ag+)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环扁桃酯是用于治疗心脑血管疾病的重要化合物,它的一种合成路线如下。
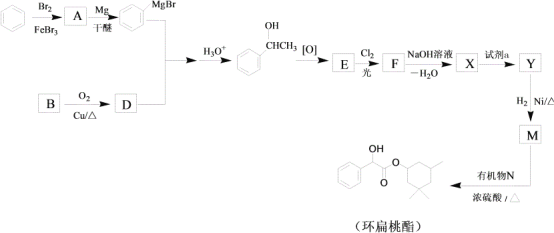
已知:RX ![]() R-MgX
R-MgX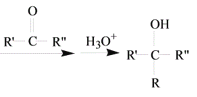 (R、R’、R”代表烃基或氢)
(R、R’、R”代表烃基或氢)
(1)A 的结构简式是___________________
(2)B → D 的化学方程式是________________
(3)红外吸收光谱表明 E 有 C=O 键。 F 的分子式为 C8H6Cl2O 。
①E 的结构简式是________
②E → F 的反应类型是________
(4)X 的结构简式是________
(5)试剂 a 是________
(6)生成环扁桃酯的化学方程式是________
(7)以 CH3CH=CH 2 、 CH3CHO 为有机原料, 结合题目所给信息 ,选用必要的无机试剂合成 CH2=CHCH=CHCH3,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)![]() B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
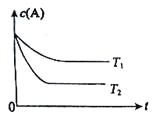
(1)上述反应的温度T1___ T2,平衡常数K(T1)___K(T2)。(填“大于”、“小于” 或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为_______。
②反应的平衡常数K=______。
③反应在0~5min区间的平均反应速率v(A)=_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com