
| A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) 放热反应 |
| B.2CO(g)+O2(g)=2CO2(g) 放热反应 |
| C.CaCO3(s)=CaO(s)+CO2 吸热反应 |
| D.H+(aq)+OH-(aq)=H2O(l) 放热反应 |
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:不详 题型:单选题

| A.反应O3+O=2O2的ΔH=E1-E3 |
| B.反应O3+O=2O2的ΔH=E2-E3 |
| C.O3+O=2O2是吸热反应 |
| D.ΔH=ΔH1+ΔH2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢氧化钾与硫酸的反应 |
| B.锌与盐酸反应放出氢气 |
| C.镁条在空气中燃烧 |
| D.Ba(OH)2·8H2O与NH4Cl反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.C(s)+ O2(g)=CO(g)ΔH=-393.5 kJ·mol-1 O2(g)=CO(g)ΔH=-393.5 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(g)ΔH=+571.6 kJ·mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.3 kJ·mol-1 |
D. C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)ΔH=-1 400 kJ·mol-1 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)ΔH=-1 400 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该过程是将太阳能转化为化学能的过程 |
| B.催化剂a表面发生氧化反应,有O2产生 |
| C.催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D.催化剂b表面的反应是CO2+2H++2e-=HCOOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


 2CO2(g)+N2(g),已知该反应在570K时的平衡常数为1×1059,但反应速率极慢。下列说法正确的是:________
2CO2(g)+N2(g),已知该反应在570K时的平衡常数为1×1059,但反应速率极慢。下列说法正确的是:________| A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| B.提高尾气净化效率的常用方法是升高温度 |
| C.增大压强,上述平衡右移,故实际操作中可通过增压的方式提高其净化效率 |
| D.提高尾气净化效率的最佳途径是使用高效催化剂 |

 Ni(CO)4(g),镍与CO反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2除去CO,生成物为S和CO2。已知相关反应过程的能量变化如图所示
Ni(CO)4(g),镍与CO反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2除去CO,生成物为S和CO2。已知相关反应过程的能量变化如图所示

 2N2(g)+3H2O(g)△H<0。为提高氮氧化物的转化率可采取的措施是(任意填一种)____________________。
2N2(g)+3H2O(g)△H<0。为提高氮氧化物的转化率可采取的措施是(任意填一种)____________________。
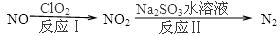
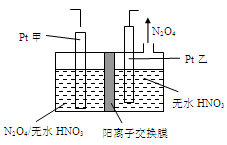
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C2H4(g) ΔH2=-Q2
C2H4(g) ΔH2=-Q2| A.ΔH<0 | B.Q2>Q1 | C.ΔH=2(Q1-Q2) | D.ΔH=Q1-Q2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C(s)+O2(g)=CO2(g)ΔH=+393.5 kJ/mol |
| B.2SO+O2=2SO3ΔH=-196.6 kJ/mol |
| C.H2(g)+1/2O2(g)=H2O(l)ΔH=-285.8 kJ/mol |
| D.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com