
【题目】在一定条件下发生反应:4NO2(g)+O2(g)![]() 2N2O5(g) ΔH<0,T1时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如表所示。
2N2O5(g) ΔH<0,T1时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如表所示。
时间/s | 0 | 5 | 10 | 15 |
c(NO2)/(mol·L-1) | 4.00 | 2.52 | 2.00 | c3 |
c(O2)/(mol·L-1) | 1.00 | c1 | c2 | 0.50 |
(1)0~10s内N2O5的平均反应速率为___,此温度下的平衡常数为___。
(2)其他条件不变,将容器体积压缩一半,则重新达到平衡时c(N2O5)___2.00mol·L-1(填“>、<或=”,下同)
(3)假设温度T1时平衡常数为K1,温度T2时平衡常数为K2,若K1<K2,则T1__T2。
(4)改变哪些措施可以增加NO2的平衡转化率___(答出任意两条即可)
(5)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol1
2C(s)+O2(g)=2CO(g) ΔH=﹣221.0kJ·mol1
C(s)+O2(g)=CO2(g) ΔH=﹣393.5kJ·mol1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=___kJ/mol。
【答案】0.1mol·L-1·s-1 0.125或1/8 > > 增加O2浓度、降低温度、增大压强、及时分离N2O5 ﹣746.5
【解析】
(1)根据v=![]() 和v(N2O5)=
和v(N2O5)=![]() v(NO2)计算可得;结合化学平衡常数为平衡时生成物浓度幂之积与反应物浓度幂之积之比可得;(2)根据压强对化学平衡的影响分析;(3)根据温度对化学平衡常数的影响分析;(4)根据影响化学平衡的因素分析可得;(5)根据盖斯定律③×2-①-②可得。
v(NO2)计算可得;结合化学平衡常数为平衡时生成物浓度幂之积与反应物浓度幂之积之比可得;(2)根据压强对化学平衡的影响分析;(3)根据温度对化学平衡常数的影响分析;(4)根据影响化学平衡的因素分析可得;(5)根据盖斯定律③×2-①-②可得。
(1)根据方程有:v(N2O5)=![]() v(NO2),故0~10s内N2O5的平均反应速率为
v(NO2),故0~10s内N2O5的平均反应速率为![]() ×
×![]() =0.1molL-1s-1;由图表,c1=1-
=0.1molL-1s-1;由图表,c1=1-![]() ×(4-2.52)=0.63,c2=1-
×(4-2.52)=0.63,c2=1-![]() ×(4-2)=0.5,15s时氧气认为0.5mol/L,故10s反应达到平衡,平衡时N2O5的浓度为
×(4-2)=0.5,15s时氧气认为0.5mol/L,故10s反应达到平衡,平衡时N2O5的浓度为![]() ×(4-2)mol/L=1mol/L,此温度下的平衡常数为
×(4-2)mol/L=1mol/L,此温度下的平衡常数为![]() =0.125;故答案为:0.1mol·L-1·s-1;0.125或1/8;
=0.125;故答案为:0.1mol·L-1·s-1;0.125或1/8;
(2)其他条件不变,将容器体积压缩一半,平衡如果不移动,则c(N2O5)=2.00molL-1,压缩体积相当于增大压强,该反应气体分子数减少,平衡正向移动,则重新达到平衡时c(N2O5)>2.00molL-1;故答案为:>;
(3)该反应是放热反应,温度升高有利于逆反应,化学平衡常数减小,温度T1时平衡常数为K1,温度T2时平衡常数为K2,若K1<K2,故T1>T2;故答案为:>;
(4)增加O2浓度、降低温度、增大压强、及时分离N2O5可以增加NO2的平衡转化率;故答案为:增加O2浓度、降低温度、增大压强、及时分离N2O5;
(5)已知:①N2(g)+O2(g)=2NO(g)△H=+180.5kJmol-1
②2C(s)+O2(g)=2CO(g)△H=-221.0kJmol-1
③C(s)+O2(g)=CO2(g)△H=-393.5kJmol-1
根据盖斯定律③×2-①-②可得:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJ/mol;故答案为:-746.5。


 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
B元素原子的核外p电子数比s电子数少1 |
C元素基态原子p轨道有两个未成对电子 |
D原子的第一至第四电离能分别是: Ⅰ |
E原子核外所有p轨道全满或半满 |
F在周期表的第8纵列 |
(1)某同学根据上述信息,推断A基态原子的核外最子排布为了![]() ,该同学所画的电子排布图违背了___________。
,该同学所画的电子排布图违背了___________。
(2)![]() 元素的电负性_____
元素的电负性_____![]() 填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于”![]() 元素的电负性。
元素的电负性。
(3)![]() 基态原子中能量最高的电子,其电子云在空间有__________个方向。
基态原子中能量最高的电子,其电子云在空间有__________个方向。
(4)下列关于F原子的价层电子排布图正确的是___________。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(5)基态![]() 离子核外电子排布式为_____________。
离子核外电子排布式为_____________。
(6)元素铜与镍的第二电离能分别为:![]() ,
,![]() ,
,![]() 原因是_________。
原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用序号填空:
①13C与14C ②正丁烷与异丁烷
③CH3CH3与CH3CH2CH3 ④
(1)属于同位素的是______;
(2)属于同系物的是______;
(3)属于同分异构体的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,将足量的BaSO4固体溶于50mL水中,充分搅拌,慢慢加入Na2CO3固体,搅拌,溶液中随c(CO32-)增大时c(Ba2+)变化曲线如下图。则下列说正确的是

A. 20℃时Ksp(BaSO4)>Ksp(BaCO3)
B. 加入Na2CO3固体立即有BaCO3固体生成
C. BaCO3的Ksp=2.5×10-10
D. 曲线BC段内,c(CO32-):c(SO42-)=25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定环境中能大量共存的是( )
A.在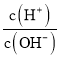 =1013的溶液中:NH4+、Ca2+、Cl-、K+
=1013的溶液中:NH4+、Ca2+、Cl-、K+
B.由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、K+
C.无色溶液中可能大量存在Al3+、NH4+、Cl-、S2-
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是( )
A. 已知2H2(g)+O2(g) =2 H2O(g) △H=-483.6kJ·mol-1,则氢气的燃烧热△H=-241.8 kJ/mol
B. 已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2
C. 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq) = CH3COONa(aq) + H2O(l) △H =-57.4kJ·mol-1
D. CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+566.0 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向IL0.1mol/LNH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发),下列说法不正确的是

A.M点溶液中水的电离程度比原溶液小
B.在M点时,n(OH-)-n(H+)=(a-0.05)mol
C.随者NaOH的加入,c(H+)/c(NH4+)不断增大
D.当n(NaOH)=0.1mol时,c(OH-)>c(Cl-)-c(NH3·H20)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:
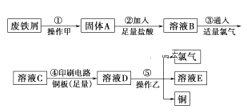
请回答下列问题:
(1)步骤①中先加入热的Na2CO3溶液除油污,操作甲的名称是_____。
(2)步骤②中,除发生反应Fe+2HCl=FeCl2+H2↑外,其他可能反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O和____。
(3)溶液C的颜色是____,溶液D中可能含有的金属阳离子有___。
(4)可以验证溶液B中是否含有Fe2+的一种试剂是____(填选项序号)。
a.稀硫酸 b.铁 c.硫氰化钾 d.酸性高锰酸钾溶液
(5)操作乙的名称是___,步骤⑤产生金属铜的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:
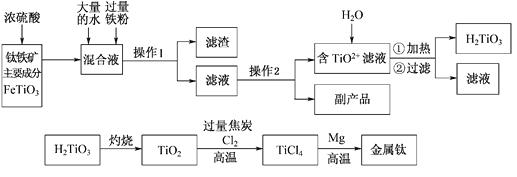
已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解。请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有________________________;
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理_____________________。
(3)已知钛的还原性介于铝与锌之间。如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是___________________________________。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式是_____________________________________。
(5)为测定溶液中TiOSO4的含量,先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。过滤后,取无色滤液20.00 mL,向其中滴加2~3滴KSCN溶液作指示剂,用______________________(填一种玻璃仪器的名称)滴加0.1000mol·L-1 FeCl3溶液,发生Ti3++Fe3+=Ti4++Fe2+。滴定终点时的现象是________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com