
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
在密闭容器中,反应X2(g)+Y2(g) 2XY(g) ΔH<0,
2XY(g) ΔH<0,
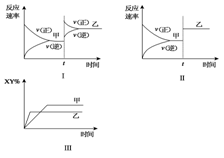
达到甲平衡时,再改变某一条件后,达到乙平衡,对此过程的分析正确的是
A.图Ⅰ是加入适当催化剂的变化情况 B.图Ⅱ是扩大容器体积的变化情况
C.图Ⅲ是增大压强的变化情况 D.图Ⅲ是升高温度的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
1993年的世界十大科技新闻称中国学者徐志傅和美国科学家穆尔共同合成了世界上最大的碳氢分子,其中一个分子由1134个碳原子和1146个氢原子构成,关于此物质说法错误的是( )
A 、是烃类化合物 B、 常温下呈固态
C、分子中可能含不饱和碳原子 D、不能在空气中燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列微粒的电子式。
C2H4 CH3— OH–
(2)键线式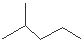 表示的分子式 ;结构简式为 ;名称是 。
表示的分子式 ;结构简式为 ;名称是 。
(3)、根据命名写出该物质的结构简式
2,3-二甲基-2-戊烯 ; 对二甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实说明HNO2为弱电解质的是:
①0.1 mol/L HNO2溶液的pH=2.1 ②常温下NaNO2溶液的pH>7
③用HNO2溶液做导电实验时,灯泡很暗 ④HNO2溶液和KCl溶液不发生反应
⑤HNO2能与碳酸钠反应制CO2 ⑥HNO2不稳定,易分解
A.①②③⑤ B.①②④⑤ C.①②⑥ D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
发展混合动力车是实施节能减排的重要措施之一。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)电解液。镍氢电池充放电原理总反应式为:
H2+2NiOOH 2Ni(OH)2。
2Ni(OH)2。
下列有关混合动力车的判断正确的是
A.在上坡或加速时,乙电极周围溶液的pH将减小
B.在上坡或加速时,溶液中的K+向甲电极迁移
C.在刹车和下坡时,甲电极的电极反应式为:2H2O+2e- H2↑+2OH-
H2↑+2OH-
D.在刹车和下坡时,乙电极增重
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)CO和H2可以合成二甲醚,化学方程式为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H<0。 如果上述反应方程式的平衡常数K值变大,则该反应_ (选填编号)。
CH3OCH3(g)+CO2(g) △H<0。 如果上述反应方程式的平衡常数K值变大,则该反应_ (选填编号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小后增大
(2)一定条件下,可以由CO2(g)和H2(g)合成CH4(g),同时还生成H2O(g)。
① 向一容积为2L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应,10min达到平衡时部分物质的浓度如下图1所示:
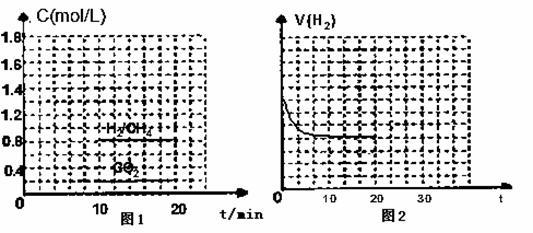
用CH4表示达到平衡时的反应速率 ,该温度下的的平衡常数等于 。
② 图2表示H2在建立平衡过程中的速率时间图,若现在20min时扩大容器体积,并在30min时又达到状态,请在图2中画出H2的逆反应方向速率时间图像。
(3)有人提出设计反应2CO=2C+O2(ΔH>0)来消除CO的污染,请判断该反应能否自发
(填“能”或“不能”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学中常借助曲线图来表示某种变化过程,如:
①平衡移动过程 ②中和滴定过程
③沉淀的生成和溶解 ④固体物质的溶解度变化过程
下列曲线图中从左到右依次表示上述过程中的
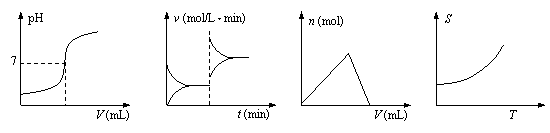

A. ①②③④ B. ②③①④ C. ④③②① D. ②①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是
①升高温度;②改用100mL 3mol/L盐酸;③多用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
A.①②④⑤ B.①③④⑤ C.①②③④ D.①②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com