
����Ŀ��700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������CO��H2O��������Ӧ��CO��g��+H2O��g��CO2��g��+H2��g����Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1����
��Ӧʱ��/min | N��CO��/mol | N��H2O��/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
����˵����ȷ���ǣ� ��
A.��Ӧ��t1min�ڵ�ƽ������Ϊv��H2����![]() molL-1min
molL-1min
B.���������������䣬��ʼʱ�������г���0.60molCO��1.20mol H2O���ﵽƽ��ʱn��CO2����0.40mol
C.���������������䣬��ƽ����ϵ����ͨ��0.20mol H2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת���ʲ��䣬H2O�������������
D.�¶�������800�棬������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ���ȷ�Ӧ
���𰸡�B
��������
A.v��CO����![]() ��
��![]() molL��1min��v��CO����v��H2����1��1����v��H2����
molL��1min��v��CO����v��H2����1��1����v��H2����![]() molL��1min����A����
molL��1min����A����
B.t1minʱ��n��CO����0.8mol��n��H2O����0.6mol��0.4mol��0.2mol��t2minʱn��H2O����0.2mol��˵��t1minʱ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬��n��CO2����n��H2����0.4mol��K��![]() ��
��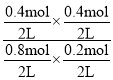 ��1����ʼ����1.2molCO��1.20molH2O������ﵽƽ��ʱn��CO2����0.40 mol����n��CO����0.6mol��0.4mol��0.2mol��n��H2O����1.2mol��0.4mol��0.8mol��n��H2����n��CO2����0.4mol��Qc��
��1����ʼ����1.2molCO��1.20molH2O������ﵽƽ��ʱn��CO2����0.40 mol����n��CO����0.6mol��0.4mol��0.2mol��n��H2O����1.2mol��0.4mol��0.8mol��n��H2����n��CO2����0.4mol��Qc�� ��1��K��˵����ʱ�ﵽ��ѧƽ��״̬�������������B��ȷ��
��1��K��˵����ʱ�ﵽ��ѧƽ��״̬�������������B��ȷ��
C.���������������䣬��ƽ����ϵ����ͨ��0.20molH2O��ƽ��������Ӧ�����ƶ����ﵽƽ��ʱCOת��������H2O���������������C����
D.800�棬��Ӧƽ�ⳣ��Ϊ0.64����B��700�棬��Ӧƽ�ⳣ��Ϊ1�������¶ȣ�ƽ�����淴Ӧ�����ƶ����÷�Ӧ�Ƿ��ȷ�Ӧ����D����
��ѡ��B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ����̼���������ܹ�ע��![]() �IJ�������Ч�������ó�Ϊ��ѧ���о�����Ҫ���⡣
�IJ�������Ч�������ó�Ϊ��ѧ���о�����Ҫ���⡣

(1)����β����������Ҫԭ��Ϊ![]() �����ܱ������з����÷�Ӧʱ��
�����ܱ������з����÷�Ӧʱ��![]() ���¶�
���¶�![]() �����������
�����������![]() ��ʱ��
��ʱ��![]() �ı仯������ͼ1ʾ���ݴ��жϣ�
�ı仯������ͼ1ʾ���ݴ��жϣ�
�ٸ÷�Ӧ��![]() ______
______![]() ����
����![]() ������
������![]() ��
��![]() ��
��
����![]() �¶��£�
�¶��£�![]() �ڵ�ƽ����Ӧ����
�ڵ�ƽ����Ӧ����![]() ______
______![]() ��
��
�۵��������������һ��ʱ������������������ѧ��Ӧ���ʡ��������ı����![]() ���ڴ����Ӧͼ�л���
���ڴ����Ӧͼ�л���![]() ��
��![]() ��
��![]() �����´ﵽƽ������еı仯����_____��
�����´ﵽƽ������еı仯����_____��
�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ͼ2��ȷ����˵����Ӧ�ڽ��е�![]() ʱ�̴ﵽƽ��״̬����______
ʱ�̴ﵽƽ��״̬����______![]() �����
�����![]() ��
��
(2)ֱ���ŷ�úȼ�ղ������������������صĻ������⡣
��úȼ�ղ����������������������![]() ����ԭ
����ԭ![]() �������������������Ⱦ��
�������������������Ⱦ��
���磺![]()
![]()
д��![]() ����ԭ
����ԭ![]() ����
����![]() ��
��![]() ��
��![]() ���Ȼ�ѧ����ʽ��______��
���Ȼ�ѧ����ʽ��______��
�ڽ�ȼú�����Ķ�����̼�������ã��ɴﵽ��̼�ŷŵ�Ŀ�ġ���ͼ3ͨ���˹�������ã���![]() ��
��![]() Ϊԭ���Ʊ�HCOOH��
Ϊԭ���Ʊ�HCOOH��![]() ��ԭ��ʾ��ͼ������b���淢���ĵ缫��ӦΪ______
��ԭ��ʾ��ͼ������b���淢���ĵ缫��ӦΪ______
�۳�����![]() ��HCOONa��ҺpHΪ10����HCOOH�ĵ��볣��
��HCOONa��ҺpHΪ10����HCOOH�ĵ��볣��![]() ______
______![]() ��д���ռ�����
��д���ռ�����![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ������ͼ��ʾ��ͬ�¶���ˮ��Һ��c(H��)��c(OH��)�Ĺ�ϵ�������ж���ȷ����( )
A.������������������c (H��) ��c (OH��)��Kw
B.T<25��
C.b���c��pH��Ϊ6����Һ������
D.ֻ�������µķ�ʽ������a����d��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ũ�Ⱦ�Ϊ0.1mol/L ����������Һ����pH �����ʾ������˵����ȷ������ ��
��� | �� | �� | �� | �� |
��Һ | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
pH | 8.8 | 9.7 | 11.6 | 10.3 |
A. ����Ũ�ȵ�CH3COOH ��HClO��Һ��pHС����HClO
B. Na2CO3��NaHCO3��Һ���������ͬ
C. ��Һˮ�ĵ���̶ȣ���>��>��>��
D. NaHCO3��Һ�У�c (Na+) =c (CO32- )+c (HCO3- )+c (H2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH��Ϊ3�������ΪV0��HA��HB��Һ���ֱ��ˮϡ�������V��pH��lg![]() �ı仯��ͼ��ʾ������������ȷ����
�ı仯��ͼ��ʾ������������ȷ����

A. ˮ�ĵ���̶ȣ�b>c>a
B. ���ֱ��õ�Ũ�ȵ�NaOH��Һ��ȫ�к�������NaOH�������b>a>c
C. ���ֱ��õ�Ũ�ȵ�NaOH��Һ��ȫ�к���������Һ��pH��a>b>c
D. ��Һ��������Ũ�ȣ� a>b>c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������±��е���Ϣ�жϣ�����˵���������
��� | ��Ӧ�� | ���� |
�� | Cl2��H2O2 | Cl�������� |
�� | Cl2��FeBr2 | FeCl3��FeBr3 |
�� | KClO3��HCl | Cl2��KCl��H2O |
A.�ڢ��鷴Ӧ����������ΪO2
B.�ڢ��鷴Ӧ��C12��FeBr2�����ʵ���֮��С�ڻ����1��2
C.�ڢ��鷴Ӧ������3mol C12��ת��6mol����
D.��������ǿ������˳��ΪC1O3�� >C12>Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
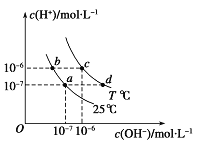
����Ŀ�������£�����![]() ��
��![]() ��Һ��
��Һ��![]() ��֪����
��֪����![]() ��̼
��̼![]() �����ķֲ�����
�����ķֲ�����![]() ƽ��ʱij������Ũ��ռ������Ũ��֮�͵ķ���
ƽ��ʱij������Ũ��ռ������Ũ��֮�͵ķ���![]() ��pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
��pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����![]()
A.����Һ��![]() ʱ����Һ�д������й�ϵ��
ʱ����Һ�д������й�ϵ��![]()
B.![]() ��Һ�д��������غ��ϵ��
��Һ�д��������غ��ϵ��![]()
C.������Һ����εμ���������ʱ![]() ��
��![]() Ũ����С
Ũ����С
D.ͨ��������֪������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����������ǿ������Һ����Ҫ��HO2-���ڡ��ҹ��о���Al-H2O2ȼ�ϵ�ؿ��������Դ�Ŀ��顢�������ȹ����Ƽ�����װ��ʾ��ͼ���¡�����˵���������
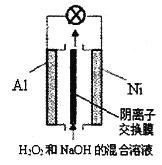
A. ��ع���ʱ����Һ��OH-ͨ�������ӽ���Ĥ��Al��Ǩ��
B. Ni���ĵ缫��Ӧʽ��HO2-+2e-+H2O=3OH-
C. ��ع��������������Һ��pH����
D. Al�缫��������13.5g����·��ͨ��9.03��1023������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����и������������FeƬ��ʴ���������˳���ǣ�������
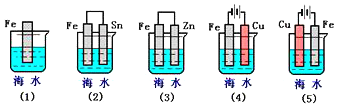
A. �ݢڢ٢ۢ� B. �ݢ٢ڢܢ� C. �ܢڢ٢ۢ� D. �ܢۢ٢ڢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com