
【题目】下列有关仪器的名称、图形、用途与使用操作的叙述均正确的是( )
选项 | A | B | C | D |
名称 | 250 mL容量瓶 | 分液漏斗 | 酸式滴定管 | 冷凝管 |
图形 |
|
|
|
|
用途与使用操作 | 配制1.0 mol·L-1NaCl溶液,定容时俯视刻度,则配得的溶液浓度小于1.0 mol·L-1 | 用甘油萃取碘水中的碘,分液时,碘层需从上口放出 | 可用于量取10.00mL 新制氯水溶液 | 蒸馏实验中将蒸气冷凝为液体 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中Fe+Cu2+===Cu+Fe2+ | 将Na加入到CuSO4溶液中2Na+Cu2+===Cu+2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应至中性2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和碘单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)在酸浸过程中会适当增大酸的浓度并不断快速搅拌,目的是______________。
(2)写出“沉镍”时发生反应的离子方程式:______________________________,当Ca2+沉淀完全时,溶液中 c(F-)> ________mol·L-1(写出计算式即可)。
(3)试剂a是一种绿色氧化剂,写出“氧化”时反应的化学反应方程式:_______________________________。
(4)操作a的内容包括过滤,洗涤,干燥。请用简洁语言描述洗涤的方法是__________________________。
(5)“调pH”时pH的调控范围为______≤PH<6.8。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正确书写下列反应的化学方程式或离子方程式。
(1)将少量的SO2气体通入足量澄清石灰水中的离子方程式:___。
(2)将过量的SO2气体通入少量氨水中的离子方程式:___。
(3)过量的铁与稀硝酸反应的离子方程式为___,该反应中稀硝酸体现___性。
(4)碳与浓硝酸反应的化学方程式为___,该反应中浓硝酸体现___性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化对工农业生产及环境保护有重要的意义。
(1)下面是氮的氧化物在几种不同情况下的转化:
①已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJ·mol-1
2SO3(g) ΔH=-196.6kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0kJ·mol-1
2NO2(g) ΔH=-113.0kJ·mol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为___。
②a.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使其反应达到平衡,正反应速率随时间变化的示意图如图1所示。反应在c点___(填“达到”或“未到”)平衡状态。
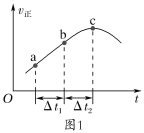
b.开始时,分别在该容器中加入Ⅰ:2molSO2(g)和2molNO2(g);Ⅱ:2molSO3(g)和2molNO(g)。则反应达到平衡时,平衡常数:Ⅰ__(填“>”“=”或“<”)Ⅱ。
(2)常温时向浓度为0.1mol·L-1体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸体积的变化曲线如图2所示,d点处两种溶液恰好完全反应。根据图2回答下列问题:
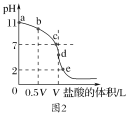
①b、c、d三点对应的溶液中,水电离的c(OH-)由大到小的顺序为____。
②滴定时,由b点到c点的过程中,下列各选项中数值保持不变的有___。
a.![]() b.
b.![]()
c.![]() d.
d.![]()
③该温度时氨水的电离平衡常数K=___。
(3)氮的氧化物易污染环境,可用氢氧化钠溶液吸收。发生的反应为:
2NaOH+NO+NO2=2NaNO2+H2O
2NaOH+2NO2=NaNO3+NaNO2+H2O
将反应混合液和氢氧化钠溶液分别加到如图3所示的电解槽中进行电解,A室产生N2。
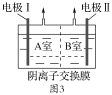
①电极Ⅱ是__极,B室产生的气体是___。
②A室NO2-发生的电极反应是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年诺贝尔化学奖授予三位分别来自法国、美国、荷兰的科学家,因其共同研究的“分子机器的设计与合成”。纳米分子机器日益受到关注,机器的“车轮”常用组件如图,下列说法正确的是( )
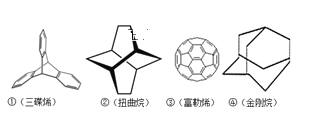
A.①②④互为同分异构体B.①②③④均属于烃
C.①②③④的一氯代物均只有3种D.①③均能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种,现取X溶液进行实验,实验过程及产物如图。下列说法正确的是
中的若干种,现取X溶液进行实验,实验过程及产物如图。下列说法正确的是![]()
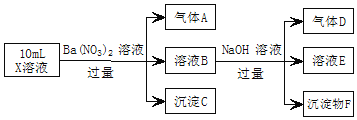
A.A是一种无色、无毒的气体
B.沉淀F为![]()
C.实验室可用排水法收集气体D
D.往溶液E中通入少量![]() ,有沉淀产生
,有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
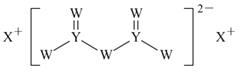
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.化合物M中W不都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备下列物质的生产流程合理的是( )
A.由铝土矿冶炼铝:铝土矿![]() Al2O3
Al2O3 ![]() AlCl3
AlCl3 ![]() Al
Al
B.由NaCl 制漂白粉:饱和食盐水![]() Cl2
Cl2![]() 漂白粉
漂白粉
C.侯德榜制碱:饱和 NaCl 溶液![]()
![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
D.从海水中提取镁:海水 ![]() Mg(OH)2
Mg(OH)2 ![]() MgO
MgO ![]() Mg
Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com