
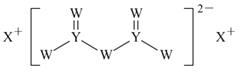
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.化合物M中W不都满足8电子稳定结构
【答案】B
【解析】
短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,为钠Na;由W、X、Y三种元素形成的化合物M的结构分析,Y形成四个共价键,说明其为Si;Y的原子序数是Z的最外层电子数的2倍,则Z为Cl;W的核外电子数与X、Z的最外层电子数之和相等,为O;依此答题。
经分析,X为Na,Y为Si,Z为Cl,W为O,则:
A.O、Si、Cl三种元素非金属性最强的为Cl,A错误;
B.单质Si为原子晶体,单质Na是金属晶体,单质Si的熔点高于单质Na,B正确;
C.O的非金属性比Si强,所以O的氢化物的稳定性比Si的氢化物强,C错误;
D.化合物M中O都满足8电子结构,D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】现有下列八种物质:①铝 ②![]() 溶液 ③蔗糖固体 ④稀硫酸 ⑤熔融的
溶液 ③蔗糖固体 ④稀硫酸 ⑤熔融的![]() ⑥
⑥![]() 饱和溶液 ⑦
饱和溶液 ⑦![]() ⑧新制备的氢氧化铁胶体分散系
⑧新制备的氢氧化铁胶体分散系
(1)上述物质属于非电解质的有_________(填序号)。
(2)上述物质能导电且属于电解质的有_________(填序号)。
(3)若将⑥滴入下列物质中,能形成⑧的是_________(填字母代号)。
A.![]() 浓溶液 B.
浓溶液 B.![]() 浓溶液 C.冷水 D.沸水
浓溶液 C.冷水 D.沸水
(4)可利用哪种效应鉴别⑥和⑧:______________________。
(5)⑦和足量②反应的离子方程式为______________________。
(6)①与⑤的水溶液反应的离子方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器的名称、图形、用途与使用操作的叙述均正确的是( )
选项 | A | B | C | D |
名称 | 250 mL容量瓶 | 分液漏斗 | 酸式滴定管 | 冷凝管 |
图形 |
|
|
|
|
用途与使用操作 | 配制1.0 mol·L-1NaCl溶液,定容时俯视刻度,则配得的溶液浓度小于1.0 mol·L-1 | 用甘油萃取碘水中的碘,分液时,碘层需从上口放出 | 可用于量取10.00mL 新制氯水溶液 | 蒸馏实验中将蒸气冷凝为液体 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图:电流计的指针会偏转,M极变粗,N极变细符合这种现象的是

A. M是铜,N是锌,R是硫酸溶液
B. M是锌,N是铜,R是硫酸铜溶液
C. M是银,N是锌,R是硝酸银溶液
D. M是铁,N是铜,R是硝酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知X为一种常见酸的浓溶液,能使蔗糖粉末变黑,A与X反应的转化关系如图所示,其中反应条件及部分产物均己略去,则下列有关说法正确的是
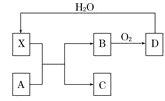
A. X使蔗糖变黑的现象主要体现了 X的强氧化性
B. 若A为铁,则A与X在室温下不会反应
C. 若A为碳单质,则将C通入少量的澄淸石灰水中,溶液仍然澄清
D. 工业上在高温、常压和使用催化剂的条件下,可以使B完全转化为D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组拟探究CO2和锌粒反应是否生成CO,已知CO能与银氨溶液反应产生黑色固体。实验装置如图所示:
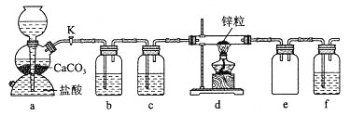
下列说法正确的是( )
A.实验开始时,先点燃酒精灯,后打开活塞K
B.b、c、f中试剂依次为饱和碳酸钠溶液、浓硫酸、银氨溶液
C.装置e的作用是收集一氧化碳气体
D.用上述装置(另择试剂)可以制备氢气并探究其还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2-甲基-1,3-丁二烯是一种重要的化工原料。可以发生以下反应。
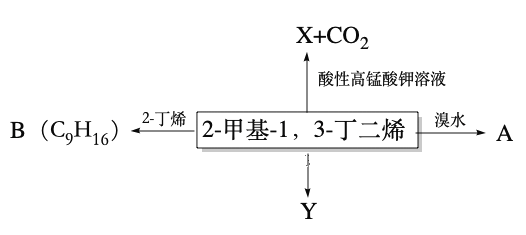
已知:
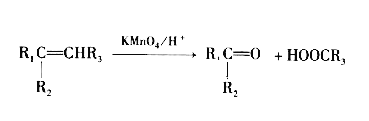
请回答下列问题:
(1)2-甲基-1,3-丁二烯与溴水发生加成反应。
① 完全加成所得有机产物的结构简式______________________________;
② 发生1,2-加成所得有机产物的化学方程式为 __________________________________;
③ 发生1,4-加成反应的名称为__________________。
(2)B为含有六元环的有机物,写出2-甲基-1,3-丁二烯与2-丁烯反应的化学方程式___________________________ 。
(3)Y(![]() )是天然橡胶的主要成分,能发生的反应有___________填标号)。
)是天然橡胶的主要成分,能发生的反应有___________填标号)。
A.加成反应 B.氧化反应 C.消去反应 D.酯化反应
(4)X的分子式为C3H4O3,其结构简式为_________________; X与丙醇发生酯化反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1molCnH2n分子中含共用电子对的数目为3nNA
B.标准状况下,11.2LCCl4中含有共用电子对的数目2NA
C.1L0.5mol/LNaHCO3溶液中所含HCO3-与CO32-数目之和为0.5NA
D.1mol/LFeCl3溶液中Fe3+数目小于1.0NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:

(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的元素是________。
(2)C元素在元素周期表中的位置是第三周期第________族。
(3)最高价氧化物的水化物酸性最强的是________,呈两性的是________。
(4)A分别与E、G、H形成的化合物中,最稳定的是________。
(5)在B、C、E、F中,原子半径最大的是________。
(6)B、H两种元素所形成的化合物所含的化学键类型为________________。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:__________________________。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com