
【题目】2-甲基-1,3-丁二烯是一种重要的化工原料。可以发生以下反应。
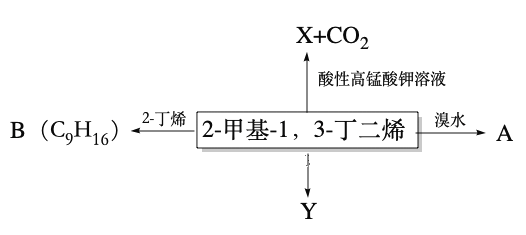
已知:
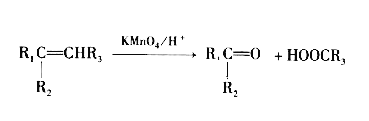
请回答下列问题:
(1)2-甲基-1,3-丁二烯与溴水发生加成反应。
① 完全加成所得有机产物的结构简式______________________________;
② 发生1,2-加成所得有机产物的化学方程式为 __________________________________;
③ 发生1,4-加成反应的名称为__________________。
(2)B为含有六元环的有机物,写出2-甲基-1,3-丁二烯与2-丁烯反应的化学方程式___________________________ 。
(3)Y(![]() )是天然橡胶的主要成分,能发生的反应有___________填标号)。
)是天然橡胶的主要成分,能发生的反应有___________填标号)。
A.加成反应 B.氧化反应 C.消去反应 D.酯化反应
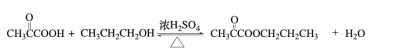
(4)X的分子式为C3H4O3,其结构简式为_________________; X与丙醇发生酯化反应的化学方程式为_____________________。
【答案】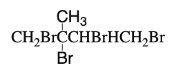
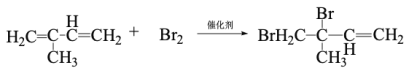 2-甲基-1,4-二溴-2-丁烯
2-甲基-1,4-二溴-2-丁烯 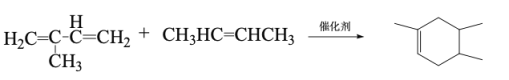 AB
AB 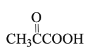
【解析】
由信息可知2-甲基-1,3-丁二烯用酸性高锰酸钾溶液氧化得到X为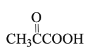 ;2-甲基-1,3-丁二烯与溴水完全加成得到
;2-甲基-1,3-丁二烯与溴水完全加成得到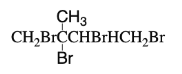 ,2-甲基-1,3-丁二烯与溴水发生1,2-加成得到
,2-甲基-1,3-丁二烯与溴水发生1,2-加成得到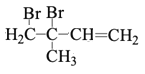 ,发生1,4-加成得到BrCH2C(CH3)=CHCH2Br;2-甲基-1,3-丁二烯与2-丁烯反应得到B(C9H16),属于加成反应,且B为含有六元环的有机物,则B为
,发生1,4-加成得到BrCH2C(CH3)=CHCH2Br;2-甲基-1,3-丁二烯与2-丁烯反应得到B(C9H16),属于加成反应,且B为含有六元环的有机物,则B为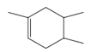 ;2-甲基-1,3-丁二烯发生加聚反应得到
;2-甲基-1,3-丁二烯发生加聚反应得到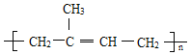 。
。
(1)①2-甲基-1,3-丁二烯与溴水完全加成所得有机产物的结构简式为 ;
;
②2-甲基-1,3-丁二烯与溴水发生1,2-加成所得有机产物为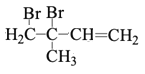 ,发生反应的化学方程式为
,发生反应的化学方程式为 ;
;
③2-甲基-1,3-丁二烯与溴水发生1,4-加成反应产物为CH2BrC(CH3)=CHCH2Br,则名称为2-甲基-1,4-二溴-2-丁烯;
(2)B为 ,2-甲基-1,3-丁二烯与2-丁烯发生加成反应的化学方程式为
,2-甲基-1,3-丁二烯与2-丁烯发生加成反应的化学方程式为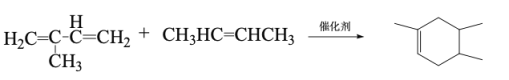 ;
;
(3) Y的结构简式为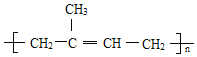 ,含有碳碳双键,可以发生加成反应,也能发生氧化反应,不能发生消去反应、酯化反应,故答案为AB;
,含有碳碳双键,可以发生加成反应,也能发生氧化反应,不能发生消去反应、酯化反应,故答案为AB;
(4) X的分子式为C3H4O3,结合信息,可知结构简式为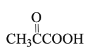 ,与丙醇发生酯化反应的化学方程式:
,与丙醇发生酯化反应的化学方程式: 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)在酸浸过程中会适当增大酸的浓度并不断快速搅拌,目的是______________。
(2)写出“沉镍”时发生反应的离子方程式:______________________________,当Ca2+沉淀完全时,溶液中 c(F-)> ________mol·L-1(写出计算式即可)。
(3)试剂a是一种绿色氧化剂,写出“氧化”时反应的化学反应方程式:_______________________________。
(4)操作a的内容包括过滤,洗涤,干燥。请用简洁语言描述洗涤的方法是__________________________。
(5)“调pH”时pH的调控范围为______≤PH<6.8。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种,现取X溶液进行实验,实验过程及产物如图。下列说法正确的是
中的若干种,现取X溶液进行实验,实验过程及产物如图。下列说法正确的是![]()
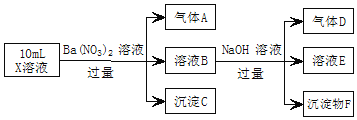
A.A是一种无色、无毒的气体
B.沉淀F为![]()
C.实验室可用排水法收集气体D
D.往溶液E中通入少量![]() ,有沉淀产生
,有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
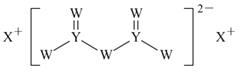
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.化合物M中W不都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.氯化铝溶液与氨水反应:Al3++3OH-=Al(OH)3↓
B.铜与氯化铁溶液反应:2Fe3++3Cu=2Fe+3Cu2+
C.氧化镁与稀硝酸反应:MgO+2H+=Mg2++H2O
D.稀硫酸与氢氧化钡溶液反应:![]() +Ba2+=BaSO4↓
+Ba2+=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。发生的反应如下:
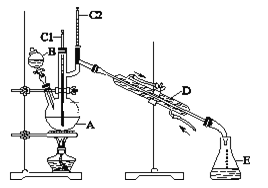
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO ,反应物和产物的相关数据列表如下:
CH3CH2CH2CHO ,反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.810 9 | 微溶 |
正丁醛 | 75.7 | 0.801 7 | 微溶 |
实验步骤如下:将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,与5 mL浓硫酸形成混合溶液,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在E中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77 ℃馏分,产量3.2g。
回答下列问题:
(1)实验中,Na2Cr2O7溶液和浓硫酸添加的顺序为__________________________。
(2)若加热后发现未加沸石,应采取的正确方法是___________________________。
(3)上述装置图中,E仪器的名称是________________________。 B使用前必须进行的操作是_____________。
(4)检验粗产品中的正丁醛的方法________________________________________。(用适当的文字和反应方程式表达)
(5)反应温度应保持在90~95 ℃,其原因是__________________________________
(6)本实验中,正丁醛的产率为_______________ %(结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备下列物质的生产流程合理的是( )
A.由铝土矿冶炼铝:铝土矿![]() Al2O3
Al2O3 ![]() AlCl3
AlCl3 ![]() Al
Al
B.由NaCl 制漂白粉:饱和食盐水![]() Cl2
Cl2![]() 漂白粉
漂白粉
C.侯德榜制碱:饱和 NaCl 溶液![]()
![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
D.从海水中提取镁:海水 ![]() Mg(OH)2
Mg(OH)2 ![]() MgO
MgO ![]() Mg
Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的![]() ,下列说法中正确的是
,下列说法中正确的是

A.阴离子的半径从大到小排列顺序为 X>Y>Z>W
B.X、Y、Z、W 元素的氢化物分子间都可以形成氢键
C.Y 的两种同素异形体在常温下可以相互转化
D.最高价氧化物对应的水化物的酸性:W>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com