
����Ŀ������98%��Ũ���ᣨ ![]() =1.84g/mL��1�����Ƴ�Ũ��Ϊ3.68mol/L��1��ϡ����500mL���밴Ҫ����գ�
=1.84g/mL��1�����Ƴ�Ũ��Ϊ3.68mol/L��1��ϡ����500mL���밴Ҫ����գ�
��1������Ũ��������ΪmL
��2���뽫���в�������ȷ��������ں����ϣ�
A����Ͳ��ȡŨ���� B�����ߵ�ҡ�� C�ý�ͷ�ιܼ�ˮ���̶��� Dϴ���ձ��ڱںͲ�����������ϴҺת������ƿ Eϡ��Ũ���� F����Һת������ƿ G������ƿ�м�����������ˮ������̶���1��2cm��
�������ȷ˳��Ϊ ��
��3��ʹ������ƿǰ��Ҫ�Ƚ��в������� ��
��4����ʵ���г������������������Һ��ʲôӰ�죿����ƫ�ߡ�ƫ�͡���Ӱ�죩
��Ũ�����ܽ��δ��ȴ�����¼����ж��� ��
�ڶ���ʱ���ӿ̶��� ��
������ǰ����ƿ����ˮ ��
���𰸡�
��1��100
��2��A��E��F��D��G��C��B
��3����©
��4��ƫ�ߣ�ƫ�ߣ���Ӱ��
���������⣺��1��Ũ��������ʵ���Ũ��c= ![]() =
= ![]() =18.4mol/L��
=18.4mol/L��
����Ҫ��ŨH2SO4�����ΪVmL������ϡ�Ͷ���CŨVŨ=CϡVϡ��֪��
18.4mol/L��VmL=3.68mol/L��500mL
��ã�V=100�����Դ��ǣ�100����2�����������Ǽ��㡢��ȡ��ϡ�͡���Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ������ȷ�IJ���˳���ǣ�AEFDGCB�����Դ��ǣ�AEFDGCB�� ��3������ƿʹ��ǰҪ�ȼ���Ƿ�©Һ�����Դ��ǣ���©�� ��4����Ũ�����ܽ��δ��ȴ�����¼����ж��ݣ�����Һ��ȴ�����ƫС����Ũ��ƫ�ߣ����Դ��ǣ�ƫ�ߣ�
�ڶ���ʱ���ӿ̶��ߣ��ᵼ����Һ���ƫС����Ũ��ƫ�ߣ����Դ��ǣ�ƫ�ߣ�
��ֻҪ�����ʱ��Һ����̶������м��ɣ�����ˮ�����Ⱦ��еĻ��Ǻ�������ģ���Ũ����Ӱ�죬���Դ��ǣ���Ӱ�죮
�����㾫�������ڱ��⿼�������һ�����ʵ���Ũ�ȵ���Һ����Ҫ�˽��������ʵ���Ũ����Һʱ�������ձ�������ˮ������ƿ�̶���1cm��2cm���ٸ��ý�Ͷ�ιܼ�ˮ���̶��߲��ܵó���ȷ�𰸣�


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڹ�����ռ����Ҫ��λ��
I.�ϳɰ���ҵ�У���ʼʱ���������������ױ�Ϊ1��3ʱ��ÿ��Ӧ1mol N2���ų�92.2kJ��������ͼΪ�ϳɰ���Ӧ�ڲ�ͬ�¶Ⱥ�ѹǿ��ʹ����ͬ���������£�ƽ�������а������������
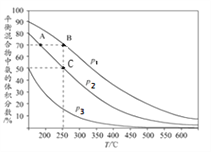
����ͼ��֪��p1��p2��p3�Ĵ�С��ϵΪ________,������_____________________________
��A��B�����ɰ��������ʴ�С��ϵΪ_____________��C�㣬N2��ת����Ϊ_____��
�����й��ںϳɰ���˵����ȷ��_________ (�����)��
A.�Ͽ�1��N��N����ͬʱ��6��N��H���γɣ���Ӧһ���ﵽƽ��״̬
B.��������ƽ����Է����������ٸı�״̬����Ӧһ���ﵽƽ��״̬
C.���ڡ�H<0����S>0���ʺϳɰ���Ӧһ�����Է�����
D.����n(N2):n(H2)�ı�ֵ������������H2��ת����
II.�������Simons�ȿ�ѧ�ҷ����˲���ʹ�����ѻ�Ϊ��Ϳ�ֱ������ȼ�ϵ�صķ��������ط�ӦΪ4NH3+3O2==2N2+6H2O��д�������ĵ缫��Ӧʽ��__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���ʹ���Ը��������Һ��ɫ�������ܷ�����ѧ��Ӧʹ��ˮ��ɫ���ǣ� ��
A.��ϩ
B.��
C.�ױ�
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�һ�����ܱ������У�����һ������һ������������̼������ѧ��Ӧ��
C(s��+2NO(g��![]() CO2(g��+N2(g����ƽ��ʱc (NO�����¶�T�Ĺ�ϵ����ͼ��ʾ��������˵����ȷ����
CO2(g��+N2(g����ƽ��ʱc (NO�����¶�T�Ĺ�ϵ����ͼ��ʾ��������˵����ȷ����
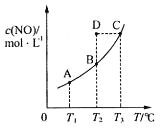
A. �÷�Ӧ����H>0
B. ���÷�Ӧ��T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1<K2
C����T2ʱ������Ӧ��ϵ����״̬D�����ʱ![]()
D����״̬B��C��D��ѹǿ�ֱ�ΪPB��PC ��PD ���� PC=PD>PB
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��8��12�գ�������������ը�¹�ȷ�����軯����NaCN�����������Ƶȣ��軯�ƶ��Ժ�ǿ����ˮ���������ж���ȼ�軯����HCN�����塣�軯��ķе�ֻ��26 ��������൱���ӷ������������ʹ���������ж��ķ��ա�ͬʱ�軯�������������ƻᷢ����ը���ش���������:
��1��д���軯����ˮ�����軯����������ӷ���ʽ_________________________
��2����ը�ֳ�Լ700�ֵ��軯�ƴ�Լ��Ҫ900�ֵ�˫��ˮ���������軯����˫��ˮ�������ͷų�����ͬʱ������ɫ���壬ʹ���軯�ƵĶ��Դ�ͣ�д���軯����˫��ˮ��Ӧ�Ļ�ѧ����ʽ________________________________��
��3����ը�����ڷ�ˮ�е�CN��������Cr2O![]() �������ⶨ�������̽��з�ˮ������
�������ⶨ�������̽��з�ˮ������

������������ˮ��������Ҫʹ�õķ�����____________
a����������������b���кͷ���������c����������������d��������ԭ��
�ڢ��з�Ӧ��������ų����÷�Ӧ�����ӷ���ʽΪ_________________��
�۲�����У�ÿ����0.4 mol Cr2O![]() ʱת�Ƶ���2.4 mol���÷�Ӧ�����ӷ���ʽ_________��
ʱת�Ƶ���2.4 mol���÷�Ӧ�����ӷ���ʽ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڹ�����ռ����Ҫ��λ��
I.�ϳɰ���ҵ�У���ʼʱ���������������ױ�Ϊ1��3ʱ��ÿ��Ӧ1mol N2���ų�92.2kJ��������ͼΪ�ϳɰ���Ӧ�ڲ�ͬ�¶Ⱥ�ѹǿ��ʹ����ͬ���������£�ƽ�������а������������
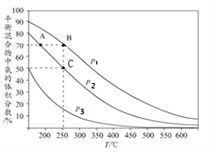
����ͼ��֪��p1��p2��p3�Ĵ�С��ϵΪ________,������_____________________________
��A��B�����ɰ��������ʴ�С��ϵΪ_____________��C�㣬N2��ת����Ϊ_____��
�����й��ںϳɰ���˵����ȷ��_________ (�����)��
A.�Ͽ�1��N��N����ͬʱ��6��N��H���γɣ���Ӧһ���ﵽƽ��״̬
B.��������ƽ����Է����������ٸı�״̬����Ӧһ���ﵽƽ��״̬
C.���ڡ�H<0����S>0���ʺϳɰ���Ӧһ�����Է�����
D.����n(N2):n(H2)�ı�ֵ������������H2��ת����
II.�������Simons�ȿ�ѧ�ҷ����˲���ʹ�����ѻ�Ϊ��Ϳ�ֱ������ȼ�ϵ�صķ��������ط�ӦΪ4NH3+3O2==2N2+6H2O��д�������ĵ缫��Ӧʽ��__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Ҫ�ɷ�Ϊ�Ȼ��ƣ�����Ϊ��������ɳ�Ϳ����Ե�MgCl2��CaCl2��Na2SO4 �� ijУ��ѧ��ȤС����̽��ʳ�εľ��ƹ��̣��Ըô���Ϊԭ�ϣ���Ʒ���������ͼ�� 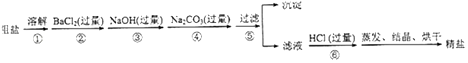
��1���ڢڲ�������Ŀ���dz�ȥ�����е����ѧʽ����ͬ����
��2���ڢݲ������ˡ������еõ������ijɷ��У���ɳ��BaSO4��Mg��OH��2�����ѧʽ��
��3��д���ڢ��漰��������ѧ��Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���������д�ڿո��У�
��1��0.5molNaOH��������g��10gNaOH�����ʵ�����mol��
��2���ڱ�״����0.5molH2�����ΪL���ڱ����5.6LH2�����ʵ���Ϊmol��
��3����58.5gNaCl����ˮ���Ƴ�500mL��Һ������Һ�����ʵ����ʵ���Ũ��Ϊ��ȡ����Һ100mL������Na+�����ʵ���Ũ��Ϊ �� Na+�����ʵ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ұ��ҵ�ϣ����������Ȼ�ԭ���ƵõĽ������ǣ� ��
A.Na��Fe��Al
B.Na��K��Zn
C.Fe��Cu��Ag
D.Na��Ca��K
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com