
 在75℃左右,用HgSO4做催化剂,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种:现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图所示,请回答下列问题;
在75℃左右,用HgSO4做催化剂,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种:现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图所示,请回答下列问题;分析 由图可知仪器的名称,A中碳化钙与分液漏斗中的水(或饱和食盐水)制备乙炔,B中NaOH溶液可除去杂质H2S,防止制备乙炔时催化剂中毒,F中先加固体后加液体,液体先加密度小的后加密度大的,C中水浴加热75℃,乙炔与水在HgSO4做催化剂下反应生成CH3CHO,D中水可吸收乙醛,乙醛含-CHO,可发生银镜反应或与新制氢氧化铜反应生成砖红色沉淀,以此来解答.
解答 解:(1)实验中仪器A的名称蒸馏烧瓶,A中制备乙炔,为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用饱和食盐水来代替水,
故答案为:蒸馏烧瓶; 饱和食盐水;
(2)防止制备乙炔时催化剂中毒,B中试剂为NaOH溶液,其作用为除去由A装置导出的气流中混有的H2S,
故答案为:NaOH溶液;除去由A装置导出的气流中混有的H2S;
(3)仪器D中盛放水,其作用是吸收乙醛蒸气,
故答案为:吸收乙醛蒸气;
(4)仪器F中应加入HgO和另外两种试剂,若将三者分别直接加入,按加入的先后顺序为氧化汞→水→浓硫酸.将HgO加放F中的操作方法是将蒸馏烧瓶横置,用药匙或纸槽将粉末送至底部,再慢慢竖立即可,
故答案为:氧化汞→水→浓硫酸; 将蒸馏烧瓶横置,用药匙或纸槽将粉末送至底部,再慢慢竖立即可;
(5)检验乙醛已制出的操作及现象为取D中少量溶液,加入新制氢氧化铜悬浊液加热若产生红色沉淀即可证明乙醛已生成(或取D中少量溶液,加入新制的银氨溶液加热,若产生光亮的银镜即可证明乙醛已生成),
故答案为:取D中少量溶液,加入新制氢氧化铜悬浊液加热若产生红色沉淀即可证明乙醛已生成(或取D中少量溶液,加入新制的银氨溶液加热,若产生光亮的银镜即可证明乙醛已生成).
点评 本题考查有机物的制备实验,为高频考点,把握制备原理及混合物分离提纯为解答的关键,侧重分析与实验能力的考查,注意有机物的性质及实验装置的作用、实验技能,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②③④ | C. | ②④⑤⑥ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ 其热化学方程式为:N2(g)+3H2(g)$?_{500℃/30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则1mol稀H2SO4和足量KOH反应的反应热为△H=2×(-57.3)kJ/mol | |
| D. | 同温同压下H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
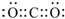 .
.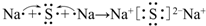 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 元素在周期表中的位置,反映了元素的原子结构和元素性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素性质.如图是元素周期表的一部分.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 需要区分的物质 | 实验方法 | |
| A | 磷酸钙和氯化铵 | 溶于水 | 与熟石灰混合研磨 |
| B | 氢氧化钠固体和熟石灰 | 将两种固体溶于水 | 溶于水,向所得溶液中分别吹入CO2气体 |
| C | 硫酸钾和碳酸钾 | 加硝酸钡溶液 | 加水溶解 |
| D | 硬水和软水 | 肥皂水 | 加热、煮沸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a<b,则c(OH-)<c(H+) | B. | 若a>b,则c(NH4+)>c(Cl-) | ||
| C. | 若a>b,则c(OH-)>c(H+) | D. | 若a=b,则c(NH4+)=c(Cl-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com