
【题目】(8分)(1)浓H2SO4能够用于干燥某些气体,是由于它具有 性;下列气体能用浓硫酸来进行干燥的气体是 (可多选,但只要有选错项,即得0分)① Cl2 ② H2S ③ NH3 ④ CO2
(2)浓H2SO4能使纸片变黑,是由于它具有 性;
(3)浓H2SO4可以与Cu反应,是由于它具有 性和 性,其反应的化学方程式是: 。
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】下列属于放热反应的是( )
A. 铝热反应 B. 煅烧石灰石(CaCO3)制生石灰(CaO)
C. C与CO2共热 D. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )
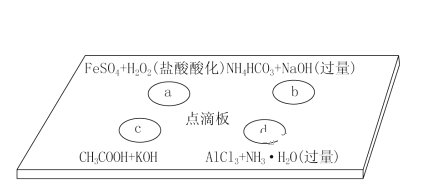
A. a反应:Fe2++2H++H2O2===Fe3++2H2O
B. b反应:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. c反应:H++OH-===H2O
D. d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图判断,下列说法正确的是

A. 2H2(g)+O2(g)=2H2O(g) △H1>0
B. 氢气的燃烧热为△H2= -241. 8kJ/mol
C. 上述A、B选项中的△H1>△H2
D. 液态水分解的热化学方程式为2H2O(l)= 2H2(g)+O2(g) △H=+571.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸铝广泛用于化工、石油等生产上,120150℃左右分解。在0℃时,溶解度为16g,100℃时,溶解度为18.4g。
首先用废铝渣制取AI(OH)3固体,流程如下:
![]()
(1)调节pH用_________试剂为好。某同学在减压过滤时,布氏漏斗内没有得到产品,可能原因是______________________。
然后将氢氧化铝和甲醛依次加入到质量分数为50%的过氧化氢溶液中(投料物质的量之比依次为1∶3∶2),装置如图1.最终可得到含甲酸铝90%以上的优质产品。反应式为:2Al(OH)3+6HCHO+3H2O2=2Al(HCOO)3+6H2O+3H2↑。

(2)反应过程可看作两步进行,第一步______________(写出化学方程式),第二步为甲酸与Al(OH)3 反应生成甲酸铝。
(3)反应温度最好控制在30—70℃之间,温度不宜过高,主要原因是_________________。
(4)实验时需强力搅拌45 min,最后将溶液____________,抽滤,洗涤,干燥得产品。可用酸性KmnO4标准溶液滴定法来测定产品纯度,滴定起始和终点的滴定管液面位置见上图2, 则消耗的酸性KmnO4标准溶液体积为__________________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿物甲由常见的三种元素组成,有如下变化。请回答下列问题:

(1)甲的化学式为_________。
(2)写出矿物甲与过量稀H2SO4/O2反应的离子方程式__________________。
(3)用文字叙述检验纯净的盐中的阳离子(写出实验操作、现象及结论)_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液与KSCN溶液混合时存在下列平衡:Fe3+(aq)+SCN-( aq) ![]() Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是
Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是

A.该反应为吸热反应
B.T1、T2时反应的平衡常数分别为K1、K2,则K1>K2
C.反应处于D点时,一定有v正大于v逆
D.A点的c(Fe3+)比B点的c(Fe3+)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,发生反应:2X(g)+Y(g) ![]() 2Z(g) ΔH=-197kJ·mol-1,若将2mol X和1mol Y充入2L的恒容密闭容器中,反应10min,测得X的物质的量为1.4mol,下列说法正确的是( )
2Z(g) ΔH=-197kJ·mol-1,若将2mol X和1mol Y充入2L的恒容密闭容器中,反应10min,测得X的物质的量为1.4mol,下列说法正确的是( )
A.10min内,反应放出的热量为197kJ热量
B.10min内,X的平均反应速率为0.06mol·L-1·min-1
C.第10min时,Y的反应速率小于0.015mol·L-1·min-1(假如体系温度不变)
D.第10min时,Z浓度为0.6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向1.0 L密闭容器中加入0.60 mol X(g),发生反应X(g)![]() Y(s)+2Z(g) ΔH>0,测得反应物X浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X浓度与反应时间的数据如下表:
反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
c(X)/mol·L-1 | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.037 5 |
(1)3 min时用Z表示的平均反应速率v(Z)=________________________。
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是______________。
由此规律推出反应在6 min时反应物的浓度a为__________ mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com