
二甲醚(CH3OCH3)被称为21世纪的新型燃料,在未来可能替代汽车燃油、石油液化气、城市煤气等,市场前景极为广阔。它清洁、高效,具有优良的环保性能。
工业上制二甲醚是在一定温度(230~280 ℃)、压强(2.0~10.0 MPa)和催化剂作用下进行的,反应器中发生了下列反应。
CO(g)+2H2(g) CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CO(g)+H2O(g) CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 ③
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 ③
(1)反应器中的总反应可表示为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
(2)二氧化碳是一种重要的温室气体,减少二氧化碳的排放是解决温室效应的有效途径。目前,由二氧化碳合成二甲醚的研究工作已取得了重大进展,其化学反应方程式为2CO2(g)+6H2(g)??CH3OCH3(g)+3H2O(g) ΔH>0。
该反应在恒温、体积恒定的密闭容器中进行,下列不能作为该反应已达到化学平衡状态的判断依据的是________。
A.容器内混合气体的密度不变
B.容器内混合气体的压强保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内消耗2 mol CO2的同时消耗1 mol二甲醚
(3)二甲醚气体的燃烧热为1 455 kJ·mol-1,工业上用合成气(CO、H2)直接或间接合成二甲醚。下列有关叙述正确的是________。
A.二甲醚分子中含共价键
B.二甲醚作为汽车燃料不会产生污染物
C.二甲醚与乙醇互为同系物
D.表示二甲醚燃烧热的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 455 kJ·mol-1
(4)绿色电源“直接二甲醚燃料电池”的工作原理示意图如图所示:正极为________(填“A电极”或“B电极”),写出A电极的电极反应式:________________________________________。
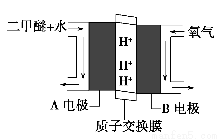
(1)-246.1 kJ·mol-1 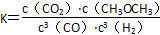 升高 (2)A (3)A (4)B电极 CH3OCH3+3H2O-12e-=2CO2+12H+
升高 (2)A (3)A (4)B电极 CH3OCH3+3H2O-12e-=2CO2+12H+
【解析】 (1)根据盖斯定律,ΔH=2ΔH1+ΔH2+ΔH3=-246.1 kJ·mol-1,增大压强,平衡向正反应方向移动,二甲醚的产率升高。(2)该反应特点是,所有反应物和产物都是气态,正反应是气体分子数减小的反应,正反应吸热。恒容条件下,密度始终不变,A选项错误;正反应是气体分子数减小的反应,压强不改变时表明反应达到平衡状态,B选项正确;气体摩尔质量等于质量与物质的量之比,当物质的量不变时,气体平均摩尔质量也不变,反应达到平衡状态,C选项正确;由反应式的化学计量数知,单位时间内消耗2 mol CO2,必生成1 mol CH3OCH3,即二甲醚的消耗速率等于其生成速率,反应达到平衡状态,D选项正确。(3)CH3OCH3分子中只存在碳氢键、碳氧键,它们都是共价键,A选项正确;二甲醚含碳、氢、氧元素,燃烧时仍然会产生CO、CO2等大气污染物,B选项错误;CH3OCH3与CH3CH2OH分子式相同,结构不同,互为同分异构体,C选项错误;燃烧热强调生成的水为液态,正确的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH=-1 455 kJ·mol-1,D选项错误。(4)从电池装置图看,A电极通入二甲醚和水,B电极通入氧气,该燃料电池中,二甲醚是还原剂,发生氧化反应,A极为负极;氧气发生还原反应,B电极为正极。负极反应式为CH3OCH3-12e-+3H2O=2CO2+
12H+。


科目:高中化学 来源:2014年高一下学期化学必修2 1-1-3 核素练习卷(解析版) 题型:选择题
钛(Ti)元素的同位素有 Ti
Ti Ti
Ti Ti
Ti Ti
Ti Ti,下列说法中不正确的是( )。
Ti,下列说法中不正确的是( )。
A.上述同位素中,Ti原子核中的中子数不可能是30
B.题述中包括5种钛元素,且质子数都是22
C.题述中包括5种钛原子,即钛的5种核素
D.钛的相对原子质量不可能为46,也不可能为50
查看答案和解析>>
科目:高中化学 来源:2014年江苏省南通市业水平测试(必修)化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列判断正确的是
A.标准状况下,22.4 L苯中含有的分子数目为NA
B.25℃、101 kPa时,20 g SO3中含有的原子数目为NA
C.1 L 1 mol·L-1 MgCl2溶液中含有的氯离子数目为NA
D.16.8 g Fe与足量水蒸气反应,转移的电子数目为0.9NA
查看答案和解析>>
科目:高中化学 来源:2014年江苏省南通市业水平测试(必修)化学试卷(解析版) 题型:选择题
下列气体中,既可用浓硫酸干燥,又可用固体氢氧化钠干燥的是
A.Cl2 B.SO2 C.H2 D.NH3
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练四 氧化还原反应的规律与应用练习卷(解析版) 题型:选择题
有如下变化:A An- ΔH1<0,B
An- ΔH1<0,B Bn- ΔH2<0,且ΔH1<ΔH2。下列说法中正确的是( )。
Bn- ΔH2<0,且ΔH1<ΔH2。下列说法中正确的是( )。
A.氧化性:A<B B.还原性:An-<Bn-
C.稳定性:B<A D.稳定性:An-<Bn-
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十八 探究型综合实验题练习卷(解析版) 题型:实验题
草酸(H2C2O4)是一种弱酸,在工业中有重要作用。某同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁,热水浸泡,经过滤得到溶液,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤沉淀备用,然后对生成的沉淀进行探究。
(1)草酸盐溶液呈弱碱性的原因是_____________________________________。
(2)该同学对生成的沉淀进行定性探究。
①提出合理假设。
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3:___________________________________________________________。
②基于假设2,设计实验方案,进行实验。请在下表中写出实验步骤以及预期现象和结论。限选实验试剂:
1 mol·L-1 H2SO4、0.1 mol·L-1盐酸、0.01 mol·L-1 KMnO4溶液、澄清石灰水。
实验步骤 | 预期现象和结论 |
步骤1:取少量沉淀于试管中,加入_________________________________ ________________________________ | _______________________________ _______________________________ 说明沉淀中有CaCO3 |
步骤2:_________________________ ________________________________ | ________________________________ |
(3)基于假设3,另一位同学对生成的沉淀进行定量探究。用稀盐酸溶解生成的沉淀,并加水配制成100 mL溶液。每次准确移取25.00 mL该溶液,用0.010 mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。若菠菜样品的质量为m g,则菠菜中草酸及草酸盐(以C2O42—计)的质量分数为________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十五 常见仪器的使用及实验基本操作练习卷(解析版) 题型:选择题
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]又称莫尔盐,是常用的分析试剂。实验室用FeSO4和(NH4)2SO4两种溶液混合很容易得到莫尔盐晶体。为了确定产品中Fe2+的含量,研究小组用KMnO4(酸化)溶液来滴定莫尔盐溶液中的Fe2+。滴定时必须选用的仪器有 ( )。
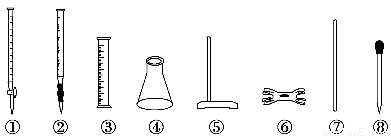
A.①④⑤⑥ B.②③⑦⑧ C.②④⑤⑥ D.④⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十三 有机物结构及同分异构体数目判断练习卷(解析版) 题型:选择题
苯环上有两个取代基的C9H12,其苯环上的一氯代物的同分异构体共有(不考虑立体异构) ( )。
A.6种 B.7种 C.10种 D.12种
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练五 元素周期表中位-构-性关系的分析练习卷(解析版) 题型:选择题
某元素X的原子的核电荷数小于18,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1。下列有关X的说法中不正确的是( )。
A.X能形成化学式为X(OH)3的碱
B.X能与某些金属元素形成化合物
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X可能形成化学式为KXO3的盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com