
钛(Ti)元素的同位素有 Ti
Ti Ti
Ti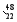 Ti
Ti Ti
Ti Ti,下列说法中不正确的是( )。
Ti,下列说法中不正确的是( )。
A.上述同位素中,Ti原子核中的中子数不可能是30
B.题述中包括5种钛元素,且质子数都是22
C.题述中包括5种钛原子,即钛的5种核素
D.钛的相对原子质量不可能为46,也不可能为50
科目:高中化学 来源:2014年高一下学期化学必修2 2-2-1 化学能转化为电能练习卷(解析版) 题型:选择题
等质量的两份锌粉a、b,分别加入两支相同的试管中,然后加入等体积等物质的量浓度且均过量的稀硫酸,同时向a中加入少量CuSO4溶液,则产生氢气的体积(V)与时间(t)的关系用图像表示如下,其中正确的是( )。
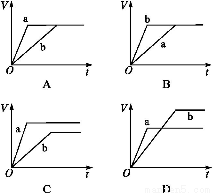
查看答案和解析>>
科目:高中化学 来源:2014年高一下学期化学必修2 1-2-3 元素周期表周期律练习卷(解析版) 题型:选择题
(双选)某元素X的原子序数为52,下列叙述正确的是( )。
A.X的主要化合价是-2、+4、+6
B.X可以形成稳定的气态氢化物
C.X的最高价氧化物对应水化物的酸性比HBrO4的酸性强
D.X的简单阴离子的还原性比溴离子强
查看答案和解析>>
科目:高中化学 来源:2014年高一下学期化学必修2 1-2-1 原子核外电子的排布练习卷(解析版) 题型:选择题
下列三种微粒可以归为一类,请选择一项可以归入此类的结构示意图( )。
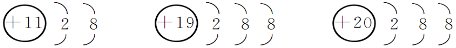
A. 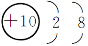 B.
B. 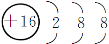
C. 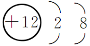 D.
D. 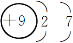
查看答案和解析>>
科目:高中化学 来源:2014年高一下学期化学必修2 1-1-3 核素练习卷(解析版) 题型:填空题
据报道,某些花岗岩会产生放射性的氡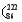 Rn),从而对人体产生伤害。请回答:
Rn),从而对人体产生伤害。请回答:
(1)该原子的质量数是 ,质子数是 ,中子数是 。
(2)请将以下Rn的原子结构示意图补全。

(3)请根据Rn的原子结构预测氡气的化学性质:
A.非常活泼,容易与氧气等非金属单质反应
B.比较活泼,能与钠等金属反应
C.不太活泼,与氮气性质相似
D.很难与其他物质发生反应
你选择 选项,理由是 。
(4)研究发现,镭能衰变为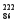 Rn,故称
Rn,故称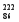 Rn为镭射气;钍能衰变为
Rn为镭射气;钍能衰变为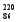 Rn,故将
Rn,故将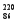 Rn称为钍射气;锕能衰变为
Rn称为钍射气;锕能衰变为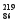 Rn,故将
Rn,故将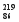 Rn称为锕射气
Rn称为锕射气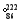 Rn
Rn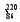 Rn
Rn Rn是 (填字母序号)。
Rn是 (填字母序号)。
A.同种元素B.同位素
C.同种核素D.同种原子
查看答案和解析>>
科目:高中化学 来源:2014年高一下学期化学必修2 1-1-2 元素的性质与原子结构练习卷(解析版) 题型:实验题
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
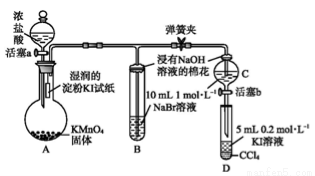
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其化学方程式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 。
(5)过程Ⅲ实验的目的是 。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 ,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源:2014年高一下学期化学必修2 1-1-2 元素的性质与原子结构练习卷(解析版) 题型:选择题
(双选)关于碱金属单质的性质叙述错误的是( )。
A.在空气中燃烧的生成物都是过氧化物
B.与水反应都能生成碱和氢气
C.熔、沸点随原子序数增加而升高
D.还原性随原子电子层数的增加而增强
查看答案和解析>>
科目:高中化学 来源:2014年高一下化学必修2 3-4-2糖类油脂蛋白质在生活中作用练习卷(解析版) 题型:选择题
生命起源的研究是世界性科技领域的一大课题。科学家认为生命起源的第一层次是产生了与硝基化合物可能是同分异构体的物质,这类物质是( )。
A.醇 B.羧酸 C.氨基酸 D.糖
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十六 基本理论综合应用题练习卷(解析版) 题型:填空题
二甲醚(CH3OCH3)被称为21世纪的新型燃料,在未来可能替代汽车燃油、石油液化气、城市煤气等,市场前景极为广阔。它清洁、高效,具有优良的环保性能。
工业上制二甲醚是在一定温度(230~280 ℃)、压强(2.0~10.0 MPa)和催化剂作用下进行的,反应器中发生了下列反应。
CO(g)+2H2(g) CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CO(g)+H2O(g) CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 ③
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 ③
(1)反应器中的总反应可表示为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
(2)二氧化碳是一种重要的温室气体,减少二氧化碳的排放是解决温室效应的有效途径。目前,由二氧化碳合成二甲醚的研究工作已取得了重大进展,其化学反应方程式为2CO2(g)+6H2(g)??CH3OCH3(g)+3H2O(g) ΔH>0。
该反应在恒温、体积恒定的密闭容器中进行,下列不能作为该反应已达到化学平衡状态的判断依据的是________。
A.容器内混合气体的密度不变
B.容器内混合气体的压强保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内消耗2 mol CO2的同时消耗1 mol二甲醚
(3)二甲醚气体的燃烧热为1 455 kJ·mol-1,工业上用合成气(CO、H2)直接或间接合成二甲醚。下列有关叙述正确的是________。
A.二甲醚分子中含共价键
B.二甲醚作为汽车燃料不会产生污染物
C.二甲醚与乙醇互为同系物
D.表示二甲醚燃烧热的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 455 kJ·mol-1
(4)绿色电源“直接二甲醚燃料电池”的工作原理示意图如图所示:正极为________(填“A电极”或“B电极”),写出A电极的电极反应式:________________________________________。
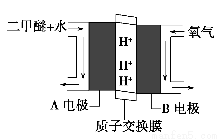
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com