
【题目】酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如下表所示:
溶解度/(g/100 g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为________________________________________,
电池反应的离子方式为________________________________________。
(2)维持电流强度为0.5 A,电池工作5分钟,理论上消耗锌________g。(已知F=96 500 C·mol-1)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过________分离回收;滤渣的主要成分是MnO2、________和________,欲从中得到较纯的MnO2,最简便的方法为________,其原理是_______________________________________________________。
【答案】(1)MnO2+H++e-===MnOOH 2MnO2+Zn+2H+===2MnOOH+Zn2+
[注:式中Zn2+可写为Zn(NH3)42+,Zn(NH3)2Cl2等,H+可写为![]() ]
]
(2)0.05
(3)加热浓缩、冷却结晶 碳粉 MnOOH 在空气中加热 碳粉转变为CO2,MnOOH氧化为MnO2
【解析】(1)酸性锌锰干电池中正极上发生还原反应,该电池放电过程中产生MnOOH,则正极反应式为MnO2+H++e-===MnOOH。金属锌做负极,发生氧化反应生成Zn2+,则负极反应式为Zn-2e-===Zn2+,结合得失电子守恒可得电池反应式为2MnO2+2H++Zn===2MnOOH+Zn2+。
(2)电流强度为I=0.5 A,时间为t=5 min=300 s,则通过电极的电量为Q=It=0.5 A×300 s=150 C,又知F=96 500 C·mol-1,故通过电子的物质的量为![]() ≈0.001 6 mol,则理论上消耗Zn的质量为 65 g·mol-1×0.001 6 mol×1/2≈0.05 g。
≈0.001 6 mol,则理论上消耗Zn的质量为 65 g·mol-1×0.001 6 mol×1/2≈0.05 g。
(3)由NH4Cl、ZnCl2的溶解度与温度的关系可知,相同温度下,ZnCl2的溶解度远远大于NH4Cl,因此从滤液中分离NH4Cl和ZnCl2,可采用加热浓缩、冷却结晶的方法。废电池的糊状填充物由碳粉、MnO2、ZnCl2和NH4Cl等组成,加水处理后,过滤,滤渣中含有碳粉、MnO2及MnOOH等,欲从中得到较纯的MnO2,可采用在空气中加强热的方法,碳粉与O2反应生成CO2,MnOOH氧化为MnO2。


科目:高中化学 来源: 题型:
【题目】纳米级Fe3O4是一种非常重要的磁性材料,同时也可用作催化剂载体和微波吸收材料。納米级Fe3O4有多种不同制法,请回答下列相关问题。
I.下图是用共沉淀法制备纳米四氧化三铁的流程。
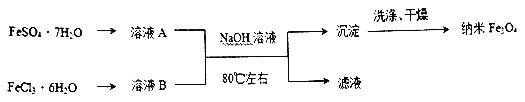
(1)除Fe3O4外铁的两种常见氧化物中在空气中性质比较稳定的是_______(填化学式),该物质的用途是___________(任写一种)。
(2)实验室保存溶液B 时为了防止出现浑浊通常采用的措施是___________ 。
(3)证明沉淀已经洗涤干净的操作是___________ 。
(4)写出该方法中发生的主要反应的离子方程式___________ 。
(5)实际生产中为提高产率,起始所用FeSO4·7H2O 和FeCl3·6H2O 的物质的量之比大于1:2,原因是___________。
II.制备纳米四氧化三铁的另一种流程如下图所示。
![]()
(6)写出第2 步反应的化学方程式______________,其中氧化产物和还原产物的物质的量之比为______。
(7)纳米Fe3O4投入分散剂中形成的分散系是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同素异形体、同位素、同系物描述的对象主体依次为( )
A.单质、原子、有机化合物B.元素、单质、化合物
C.无机化合物、元素、有机化合物D.原子核、原子、分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展,新材料层出不穷,下列不属于合金材料的是
A. 304不锈钢炊具 B. 现行流通的1元硬币
C. 古代的司母戊鼎 D. 秦皇陵墓模拟江湖的水银
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为探究MnO2与FeC13·6H2O的反应,设计了下列装置:

查阅文献有如下信息:
①FeCl3的熔点为282℃,沸点为315℃;
②FeCl3·6H2O的熔点为37℃,沸点为285℃:
③3Fe2++2[Fe(CN)6]3-==Fe3[Fe(CN)6]2↓(蓝色)。
实验过程记录:


回答下列问题:
(1)管壁内形成黄色液滴,可能的原因是_____________________。
(2)B中溶液变红,请用离子方程式解释其原因_____________。
(3)对C中溶液变棕黄色,小组展开进一步实验(如图所示):则C中溶液变棕黄色的原因是_______________。
(4)对A中残留物进行分离,其中得到一种不溶于水的红棕色固体,写出A中生成该固体的化学方程式___________________________。
(5)在A中,MnO2发生反应的化学方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,溶液的导电性(以电流I表示)滴入的稀硫酸的体积(用V表示)间的关系最接近真实情况的是( )
A.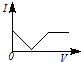
B.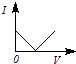
C.
D.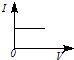
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下图两种化合物的结构或性质描述正确的是( )

A. 不是同分异构体
B. 分子中共平面的碳原子数相同
C. 均能与溴水反应
D. 可用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实不能用勒沙特列原理解释的是( )
A.新制的氯水在光照下颜色变浅
B.H2、I2、HI平衡混合气加压后颜色变深
C.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率
D.在合成氨的反应中,加压有利于氨的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:

(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________,Sn极附近溶液的pH________(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是________,总反应的离子方程式为________________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com