
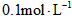 某一元酸(HA)溶液中
某一元酸(HA)溶液中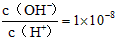 ,下列叙述正确的是
,下列叙述正确的是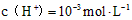
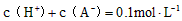
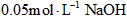 溶液等体积混合后所得溶液中
溶液等体积混合后所得溶液中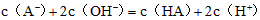
科目:高中化学 来源: 题型:阅读理解
| 实 验 混合溶液 |
A | B | C | D | E | F |
| 4mol?L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | 15 | 10 | 0 |
| 组别 | c(HA)/mol?L-1 | c(NaOH)/mol?L-1 | 混合液pH |
| 甲 | c | 0.2 | pH=7 |
| 乙 | 0.2 | 0.1 | pH>7 |
| 丙 | 0.1 | 0.1 | pH=9 |
查看答案和解析>>
科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:021
常温下,某PH=1的一元酸HA溶液中,HA的电离度为10%,某0.1mol/L的一元碱BOH溶液中[OH-]与[H+]之比为1012.将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
[ ]
A.BOH是一元强碱
B.混合后,HA的电离度仍为10%
C.混合溶液中[A-]>[B+]
D.[H+]与[A-]之比值,原HA溶液大于混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com