
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于磷化氢的相对分子质量比氨气的大,所以沸点:PH3>NH3 |
| C、若A2+2D-═2A-+D2,则氧化性D2>A2 |
| D、若R2-和M+的电子层结构相同,则离子半径R2->M+ |


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
| A、用食盐清洗热水瓶中的水垢 |
| B、漂白粉在空气中容易变质的原因是Ca(ClO)2见光分解 |
| C、加碘食盐,能使淀粉显蓝色 |
| D、氯水应避光保存,是因为HClO见光分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、②③⑤ | B、①④⑤ |
| C、①③⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
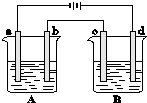 如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )
如图所示的A、B两个电解池中的电极均为铂,在A池中加入0.05mol?L-1的CuCl2溶液,B池中加入0.1mol?L-1的AgNO3溶液,进行电解.a、b、c、d四个电极上所析出的物质的物质的量之比是( )| A、1:1:2:1 |
| B、2:1:1:1 |
| C、2:2:4:1 |
| D、2:1:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol 固体NaHSO4含有的阴阳离子总数为2NA |
| B、标准状况下22.4L CH4和C2H4的混合气体所含氢原子数为4NA |
| C、常温常压下,3.4gNH3中含N-H键数目为0.6NA |
| D、56 g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2的相对分子质量为44g/mol |
| B、“物质的量”是“物质的质量”的简称 |
| C、摩尔只能用于计量纯净物 |
| D、阿伏伽德罗常数的单位是mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
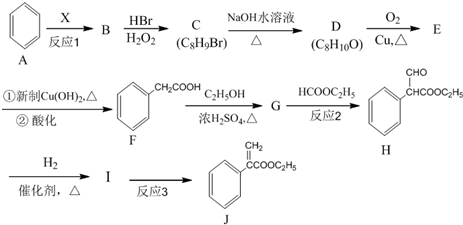
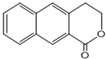 是一种重要的药物合成中间体,请结合题目所给信息,写出以
是一种重要的药物合成中间体,请结合题目所给信息,写出以 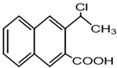 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com