
����Ŀ��ˮ������Ҫ�Ľ������ϡ�ˮ�����ϵ���Ҫ�ɷ�ΪCaO��SiO2��������һ��������������þ�Ƚ����������ʵ���Ҳⶨˮ����Ʒ�иƺ����Ĺ�����ͼ��ʾ��

�ش��������⣺
��1���ڷֽ�ˮ����Ʒ�����У�������Ϊ�ܼ����Ȼ��Ϊ���ܼ���������뼸�����ᡣ����H2O2��Ŀ����__________��
��2������A������ǿ�ᵫ����һ�����ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽΪ______________��
��3������B����Ҫ�ɷ�Ϊ_________________________���ѧʽ����
��4������Ƴ�����ϡH2SO4��������KMnO4����Һ�ζ���ͨ���ⶨ��������ɼ�ӻ�֪�Ƶĺ������ζ���ӦΪ�� ![]() +H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ
+H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ
______________��
���𰸡� ����Ʒ�п��ܴ��ڵ�Fe2+����ΪFe3+ SiO2+4HF=SiF4��+2H2O Fe(OH)3 �� Al (OH)3 45.0%
����������1��Fe3+������PH��Сʱת��Ϊ������������Ҫ��Fe2+����ΪFe3+��˫��ˮ���Խ�Fe2+����ΪFe3+�Ҳ��������µ����ʣ���2���������費����һ��������Һ�����Գ���A�Ƕ������裬������������������ᷴӦ�Ļ�ѧ����ʽΪ��SiO2+4HF=SiF4��+2H2O����3�����ȿ��Դٽ�Fe3+��Al3+ˮ��ת��ΪFe(OH)3 �� Al (OH)3��PHΪ4-5ʱCa2+��Mg2+��������Fe3+��Al3+���������Գ���BΪFe(OH)3 �� Al (OH)3��
(4) 5Ca2+��5H2C2O4��2KMnO4
n(KMnO4)=0.0500 mol/L��36.00��103 mL=1.80��103 mol
n(Ca2+)=4.50��103 mol
ˮ���иƵ���������Ϊ4.50��103 mol��40.0 g/mol��0.400 g��100%=45.0%��


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2�֣�һ���¶��£����淴Ӧ2NO2![]() 2NO+O2��������̶����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ� ��
2NO+O2��������̶����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ� ��
����λʱ��������n mol O2��ͬʱ����2n mol NO2��
����λʱ��������n mol O2��ͬʱ����2n mol NO��
��NO2��NO��O2��Ũ�ȱ�Ϊ2��2��1��
����������ѹǿ���ٸı䣻
������������ɫ���ٸı䣻
����������ƽ��Ħ���������ٸı䣮
A. �٢ܢݢ� B. �٢ڢۢ� C. �ڢۢܢ� D. ����ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���[(NH4)2CO3]�������¾����Է��طֽ��������������˵����ȷ����
A. ̼��立ֽ�����Ϊ�������ӷ������壬ʹ��ϵ��������
B. ̼��立ֽ�����Ϊ������������
C. ̼��立ֽ������ȷ�Ӧ�����������оݲ����Է��ֽ�
D. ̼���ζ����ȶ��������Է��ֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��·����ķ�Ӧ��2C2H2(g)+5O2(g)4CO2(g)+2H2O(g) ��H = -2599 kJ��mol��1��������������ȷ����
A.�÷�Ӧ�Ƿ��ȷ�ӦB.����c(O2)��K����
C.K���¶����߶���СD.��ͨ��Qc��K֮��Ĵ�С��ϵ�жϷ�Ӧ���ƶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������У�һ�������½������·�Ӧ��NO��g��+CO��g��![]()
![]() N2��g��+CO2��g����H=-373��2KJ/mol���ﵽƽ���Ϊ���NO��ת���ʺ÷�Ӧ�����ʣ��ɲ�ȡ�Ĵ�ʩ��
N2��g��+CO2��g����H=-373��2KJ/mol���ﵽƽ���Ϊ���NO��ת���ʺ÷�Ӧ�����ʣ��ɲ�ȡ�Ĵ�ʩ��
A. �Ӵ���ͬʱ�����¶�
B. �Ӵ���ͬʱ����ѹǿ
C. �����¶�ͬʱ����N2
D. �����¶�ͬʱ����ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() I�dz�����ѱ����֮һ������ͨ���ⶨ������ˮ��
I�dz�����ѱ����֮һ������ͨ���ⶨ������ˮ�� ![]() I�ĺ����仯�����˵�վ�Ƿ�������������й©�������й�
I�ĺ����仯�����˵�վ�Ƿ�������������й©�������й� ![]() I�������д�����ǣ� ��
I�������д�����ǣ� ��
A.![]() I�Ļ�ѧ������
I�Ļ�ѧ������ ![]() I��ͬ
I��ͬ
B.![]() I��������Ϊ53
I��������Ϊ53
C.![]() I��ԭ�Ӻ��������Ϊ78
I��ԭ�Ӻ��������Ϊ78
D.![]() I��ԭ�Ӻ�������������������
I��ԭ�Ӻ�������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ������ͺͻ�ѧ��������ȫ��ͬ����
A. MgCl2 NaOH B. HCl SiO2 C. NaOH NH4Cl D. ���� ���ʯ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������250mL0.1molL��1��H2SO4��Һ���ش������й����⣬�����²������裺
�ٰ���ȡ�õ�ŨH2SO4���ձ��ڻ�������ʢ��һ����ˮ��С�ձ��У����ò��������Ͻ���
�ڰѢ���������ҺС��ת������A��
�ۼ�����A�м�����ˮ��Һ���̶���1��2cm�������ý�ͷ�ι�С�ĵμ�����ˮ����Һ��Һ��ײ���̶�������
������������ˮϴ���ձ��Ͳ�����2��3�Σ�ÿ��ϴ�ӵ�Һ�嶼С��ת��A�У�������ҡ��
���ò�������A���������ҡ��
����д���пհף�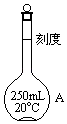
��1��д��ͼ������A������ �� ʹ�ô�����AǰӦ������Ƿ� ��
��2�������������ȷ˳��Ϊ������ţ� ��
��3��ת����Һʱ��Ӧ�Ƚ���Һ �� Ȼ����Һ�ز�����ע������A�У�
��4�����������в���ʱ����������ҺŨ�Ƚ��к�Ӱ�죨�ƫ�ߡ�ƫ�͡���Ӱ�족��
����Ͳ������ˮ����������ȡŨ������
�ڲ���ϴ��Һת��������A�Ͷ�����
�۶���ʱ����������A�̶�����
������Aֻ������ˮϴ�ӣ���δ�������������Һ ��
��5����ʵ������г����������Ӧ��δ�����
�ټ�����ˮʱ���������˿̶���
��������ƿ��ת����Һʱ��������Һ�ε�������ƿ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com