
【题目】短周期元素W、X、Y、Z分别属于三个周期,其原子序数依次增大,Y的原子半径是短周期主族元素中最大的.由W、X、Y、Z组成的物质之间存在下图所示的转化关系,其中m是元素Y的单质,n是元素Z的单质,通常为黄绿色气体,s的水溶液常用作漂白剂和消毒剂. 
请回答下列问题:
(1)Y的元素符号是 . 常温时Z的最高价氧化物对应水化物的水溶液pH7(填 大于、小于或等于).
(2)X的元素符号是 , 它位于元素周期表中第周期第族,它与同主族相邻元素相比,非金性更强的是 , 能说明这一强弱关系的事实是 .
(3)r的化学式是 , p中存在的化学键类型是 . 用电子式表示q的形成过程 .
(4)n与p反应的化学方程式是 , 该反应中2mol n完全反应时转移电子的数目是NA .
【答案】
(1)Na;小于
(2)O;二;VIA;O;H2O比H2S更稳定
(3)H2O;共价键和离子键;![]()
(4)Cl2+2NaOH=NaCl+NaClO+H2O;2
【解析】解:Y的原子半径是短周期主族元素中最大的,则Y为Na,m是元素Y的单质,故m为Na,n是元素Z的单质,通常为黄绿色气体,则n为Cl2 , Z为Cl元素,m为Na,n为Cl2 , 则生成p为NaCl,为s的水溶液常用作漂白剂和消毒剂,则s中含有ClO﹣ , 且n+p=q+r+s,即Cl2+p=NaCl+s+r(s中含ClO﹣),则为Cl2+2NaOH=NaCl+NaClO+H2O,故p为NaOH,s为NaClO,r为H2O,结合短周期主族元素W、X、Y、Z原子序数依次增大可知,W为H、X为O、Y为Na、Z为Cl,(1)(1)Y的元素符号是Na;Z的最高价氧化物对应水化物为HClO4 , 故pH小于7,所以答案是:Na;小于;(2)X的元素符号是O;故是第二周期第VIA族元素;在元素周期表中越往上越往右非金属性越强,故与同主族相邻元素相比,非金性更强的是O;能说明这一强弱关系的事实是H2O比H2S更稳定;所以答案是:O;二;VIA;O;H2O比H2S更稳定;(3)r的化学式是H2O;p为NaOH,其中氧原子和氢原子之间结合的作用力是共价键,钠离子和氢氧根离子之间之间结合的作用力是离子键,故化学键类型是共价键和离子键;q为NaCl其形成过程为 ![]() ;所以答案是:H2O;共价键和离子键;
;所以答案是:H2O;共价键和离子键; ![]() ;(4)n为Cl2 , p为NaOH,故n与p反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O;
;(4)n为Cl2 , p为NaOH,故n与p反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O;
Cl2+2NaOH=NaCl+NaClO+H2O~ | 1mole﹣ |
1 | 1 |
2 | 2 |
n(e﹣)=2mol,N(e﹣)=2mol×NA=2NA ,
所以答案是:Cl2+2NaOH=NaCl+NaClO+H2O;2.


科目:高中化学 来源: 题型:
【题目】下列关于糖类物质对应正确的是①存在于DNA而不存在于RNA的糖类;②细胞主要的能源物质;③存在于动物乳汁而不存在于肝脏细胞的糖类( )
A. 核糖、纤维素、糖原 B. 脱氧核糖、葡萄糖、乳糖
C. 核糖、葡萄糖、糖原 D. 脱氧核糖、纤维素、糖原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】英国一家公司正在研发全球首款“充一次电,用七天”的碱性氢氧燃料手机电池.如图为碱性氢氧燃料电池结构示意图. 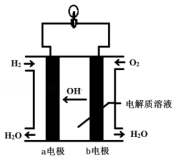
请回答下列问题.
(1)电池是将化学能直接转化为能的装置.
(2)氢氧燃料电池中发生反应的化学方程式是 . 作为碱性氢氧燃料电池,该电池的电解质溶液可以是 .
(3)b 电极上的反应为,则该电极为电池的极.从氧化还原角度分析,该反应属于反应.
(4)氢氧燃料电池与普通电池相比,其优点是(答出一点即可).但作为手机电池,长时间使用时,会感觉手机发烫,这是因为有一部分能量转化为能,所以它还需要解决一些问题,如:手机壳必须多开一个排气孔,可能的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸的电离方程式为![]()
![]()
![]() +H+,其Ka=6.25×10-5,苯甲酸钠(
+H+,其Ka=6.25×10-5,苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,H2CO3的Ka1=4.17×l0-7,Ka2=4.90×l0-11。在生产碳酸饮料的过程中,除了添加NaA外, 还需加压充入CO2气体。下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,H2CO3的Ka1=4.17×l0-7,Ka2=4.90×l0-11。在生产碳酸饮料的过程中,除了添加NaA外, 还需加压充入CO2气体。下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
A. H2CO3的电离方程式为 H2CO3![]() 2H++CO32-
2H++CO32-
B. 提高CO2充气压力,饮料中c(A-)不变
C. 当pH为5.0时,饮料中 =0.16
=0.16
D. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应X+3Y2E+2F,在甲、乙、丙、丁四种不同条件下,分别测得反应速率为甲:v(X)=0.3molL﹣1min﹣1 , 乙:v(Y)=0.3molL﹣1min﹣1 , 丙:v(E)=0.4molL﹣1min﹣1 , 丁:v(F)=0.02molL﹣1min﹣1 , 则反应速率最快的是( )
A.甲
B.乙
C.丙
D.丁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是其中的五种元素.下列说法不正确的是( ) 
A.原子半径:Y>X
B.最高价氧化物的水化物的酸性:R>W
C.气态氢化物的稳定性:X>W
D.单质与水(或酸)反应的剧烈程度:Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下,分别测得反应2SO2+O2![]() 2SO3的速率如下,其中最快的是( )
2SO3的速率如下,其中最快的是( )
A. v(SO2)=4 mol/(L·min) B. v(O2)=2 mol/(L·min)
C. v(SO2)=0.1 mol/(L·min) D. v(SO2)=0.1 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示。

(1)写出该反应的化学方程式:_______________________________________________________;
(2)0~4分钟时,A的平均反应速率为____________;
(3)到达平衡时B的转化率为____________;
(4)该反应是放热反应,恒容条件下,下列措施中能使n(A)/n(C)降低的有__________。
A.充入氦气 B.使用催化剂 C.再充入2.4mol A和1.6mol B D.降低温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com