
����Ŀ������ȩ������ˮ���������л��ܼ����ܶ�Լ����ˮ���ܶȣ��ڼ��������·����绯��Ӧ�����Ʊ�������ͱ��״�����ˮ���ܽ�Ȳ����������л��ܼ����ܶ�Լ����ˮ���ܶȣ�����Ӧԭ�����£�
2C6H5CHO+NaOH��C6H5CH2OH+C6H5COONa
C6H5COONa+HCl��C6H5COOH+NaCl
��������������������
����ȩ | ���״� | ������. | �� | |
�е�/�� | 178 | 205 | 249 | 80 |
�۵�/�� | 26 | -15 | 122 | 5.5 |
��������ˮ�е��ܽ� | ||
17�� | 25�� | 100�� |
0.21g | 0.34g | 5.9g |
ʵ���������£�

��1������������������1Сʱ����ͼ1�������м��ȹ̶�װ��δ������

����A������Ϊ___����������B��Ϊͼ2�е�����C��Ч������B����˵��ԭ��___��
��2���������йط�Һ©����ʹ�ò���ȷ����___������ĸ����
A.��Һ©����ʹ��֮ǰ�������Ƿ�©ˮ
B.��Һ©���ڵ�Һ�岻�ܹ��࣬����������
C.�����Һ©����������̨�Ͼ��ã��ֲ���������������з�Һ
D.��Һʱ���²�Һ�����������ر���������һ���ձ��ٴ�����ʹ�ϲ�Һ������
��3�����������÷�ˮԡ���������ٽ��в����ܣ���ͼ2�����ռ�___�����֡�ͼ2����һ�����Դ�����ȷ��Ӧ��Ϊ___��
��4������ʱ����ͼ3���ձ��б����ᾧ��ת�벼��©��ʱ�������ϻ�ճ���������壻��___��ϴ�����ϲ����ľ��塣������ɺ���������ˮ�Ծ������ϴ�ӣ�ϴ��ǰӦ��___��
��5���õ�����ƽȷ��ȡ0.2440g����������ƿ�м�100mL����ˮ�ܽ⣨��Ҫʱ���Լ��ȣ�������0.1000mol��L-1�ı�����������Һ�ζ��������ı�����������Һ19.20mL��������Ĵ���Ϊ___%��
���𰸡�������ƿ(��������ƿ) B�ĽӴ��������ȴ��������ȩ��Ч���� CD 205 �¶ȼƵ�ˮ������������ƿ��֧�ܿ� ��Һ ��Сˮ��ͷ 96.00%
��������
(1)��������A�������Լ��������������ƽ������BΪ���������ܣ�����CΪֱ�������ܣ���������������Ч��Ҫ����ֱ�������ܣ����������ܽӴ������
(2)�л��������ӵ�����ʹ��ǰӦ����Ƿ�©ˮ����Һ©���ڵ�Һ�岻�ܹ��࣬���÷�Һ©������Ļ����Ӧ�������ܣ����÷�Һ�ķ������룻���������������֮ǰ��Ӧʹ��Һ©������ѹǿ���,��Һ©�����ȷ��²�Һ�����ϲ�Һ��,�������²�Һ�彻�棻
(3)�ϲ�Ϊ���״��Ĵ�Ʒ�����������÷�ˮԡ�����������ܵ�Ŀ���ǵõ����״�����֣����״��е�205�棬ͼ2�¶ȼƵ�ˮ����λ�ô���
(4)���ձ��еı����ᾧ��ת�벼��©��ʱ��������������ճ���������壬��ѡ����Һ��ϴ�����ϲ����ľ��壬���پ������ʧ��������ɺ���������ˮ�Ծ������ϴ�ӣ�ϴ��Ӧ��Сˮ��ͷ��
(5)�������NaOH��Һ��������кͷ�Ӧ�����ݱ������NaOH֮��Ĺ�ϵʽ���㱽������������Ӷ����㱽���������������
(1)����װ��ͼ����֪������A������������,����Ϊ������ƿ(��������ƿ),����BΪ����������,����CΪֱ��������,B�ĽӴ������,��ȴ��������ȩ��Ч����,������������B��Ϊ����C,Ч������B��
(2)A.��Һ©�����в�������,��ʹ��֮ǰ������Ƿ�©ˮ,��A��ȷ��
B.��Һ©���ڵ�Һ�岻�ܹ���,����������,��B��ȷ��
C.����������֮ǰ,Ӧ��ʹ��Һ©�����������ϵİ��ۻ�С��©�����Ͽھ�����С��,ʹ�������ͨ,��C����
D.��Һʱ���²��Һ�����������ر������������ձ����ӷ�Һ©���Ͽڽ��ϲ�Һ�嵹������D����
����CD��
(3)�����ܵ�Ŀ���ǵõ����״������,�����ռ�205������,����ʱ,�¶ȼƲ������DZ��״��������¶�,�����¶ȼƵ�ˮ����Ӧ����������ƿ��֧�ܿڴ���
(4)���ձ��еı����ᾧ��ת�벼��©��ʱ,������������ճ����������,��ѡ��Һ�彫�ձ����ϵľ����������ת�벼��©��,Ŀ�ļ��پ������ʧ,����ѡ���ϴ��Һ��Ӧ���Dz���ʹ�����ܽ���ʧ,Ҳ����������ʵ�,ѡ������Һ����ϴ����õ�,ϴ��ʱΪϴ������,Ӧ��ϴ�Ӽ�����ͨ����ֽ,��ϴ�Ӽ��;����ֽӴ�,������ɺ���������ˮ�Ծ������ϴ��,ϴ��Ӧ��Сˮ��ͷ��
(5)���ݻ�ѧ��ӦC6H5COOH+NaOH��C6H5COONa+H2O����Ӧ����0.1mol/LNaOH��Һ19.20mL�����ʵ���Ϊ0.1mol/L��0.0192L=0.00192mol�������б����������=0.00192mol��122g/mol=0.23424g������������=0.23424g/0.2440g��100%=96.00%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ������ˮ��Һ���������������е������֣�![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ����ȡ����100mL�ĸ���Һ��������ʵ�飺
����ȡ����100mL�ĸ���Һ��������ʵ�飺
(1)��һ�ݼ�����NaOH��Һ�����ȣ��ռ�����״���µ�����448mL��
(2)�ڶ��ݼ�����![]() ��Һ���ó���
��Һ���ó���![]() ��������������ϴ�ӡ������������Ϊ
��������������ϴ�ӡ������������Ϊ![]() ��
��
��������ʵ�飬�����Ʋ���ȷ����![]()
A.![]() һ������
һ������
B.100mL����Һ�к�![]()
C.![]() ��һ������
��һ������
D.![]() ��ȷ��������ԭ��Һ�м���
��ȷ��������ԭ��Һ�м���![]() ��Һ���м���
��Һ���м���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������̿��ĩ����Ҫ�ɷ�MnO2��������Al2O3��Fe2O3�����ʣ�Ϊԭ����MnSO4��H2O�Ĺ����������£�
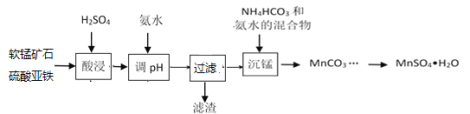
��֪��pH��3.3����Һ������Fe3+��pH��5.0����Һ������Al3+��pH��8��Mn2+��ʼ������
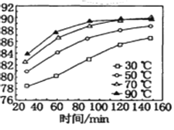
��1�����������������䣬�ڲ�ͬ�¶��¶Ժ����̿�۽���������̽�������ʱ��仯��ͼ�����������¶���ʱ��ֱ�Ϊ________�桢______min��
��2���������ʱ���ὫFe2+������Fe3+���������ķ�Ӧ���ӷ���ʽΪ__________��
��3�����ʱҪ�������ᣬ����Ũ�Ȳ��ܹ�����߹�С��������Ũ�ȹ�Сʱ��������к��ɫ�������֣�ԭ����_____________________________��
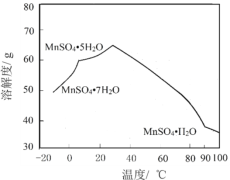
��4��MnSO4��ˮ�е��ܽ�����¶ȹ�ϵ��ͼ����MnCO3��ýϴ�����MnSO4H2O����ķ����ǣ���MnCO3����_________�������¶�Ϊ_________���Ͻᾧ���õ�MnSO4H2O���壬ϴ�ӡ���ɡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
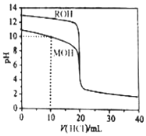
����Ŀ�������£���Ũ��Ϊ![]() ������ֱ���μ��뵽
������ֱ���μ��뵽![]() ������һԪ��MOH��ROH��Һ�У�pH��������Һ����ı仯��ͼ��ʾ������˵����ȷ����
������һԪ��MOH��ROH��Һ�У�pH��������Һ����ı仯��ͼ��ʾ������˵����ȷ����![]()
A.![]() ʱ����Һ����Ũ�ȵĹ�ϵ�ǣ�
ʱ����Һ����Ũ�ȵĹ�ϵ�ǣ�![]()
B.������MOH��ROH��Һ�������Ϻ�������ζ���MOHǡ�÷�Ӧʱ����Һ������Ũ�ȵĹ�ϵ�ǣ�![]()
C.![]() ʱ����Һ����Ũ�ȵĹ�ϵ�ǣ�
ʱ����Һ����Ũ�ȵĹ�ϵ�ǣ�![]()
D.![]() ʱ�������ܴ��ڣ�
ʱ�������ܴ��ڣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��������ͼ��ʾ�ζ����õ���Ӧ���ߡ�����˵���������( )

A.Ka2(H2C2O4)=10-4.19
B.ֱ�ߢ���X=![]()
C.��NaHC2O4��Һ��c(H2C2O4)+c(H+)=c(OH-)+c(C2O42-)
D.������ֱ�ߵ�б�ʾ�Ϊ1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬����������ʵ�飺
��ʵ��ԭ����2KMnO4 + 5H2C2O4 + 3H2SO4��K2SO4 + 2MnSO4 + 10CO2�� + 8H2O
��ʵ�����ݼ���¼��
ʵ���� | �����£��Թ��������Լ���������/mL | ��������Һ��ɫ������ɫ����ʱ��/min | |||
0.6 mol/L H2C2O4��Һ | H2O | 3 mol/L ϡ���� | 0.05mol/L KMnO4��Һ | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
��ش�
��1�������ϱ��е�ʵ�����ݣ����Եõ��Ľ�����__________________��
��2����С��ͬѧ���ݾ��������n(Mn2+)��ʱ��仯���Ƶ�ʾ��ͼ����ͼ1��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+) ��ʱ��仯������Ӧ��ͼ2��ʾ����С��ͬѧ����ͼ2��ʾ��Ϣ������µļ��裬����������ʵ��̽����
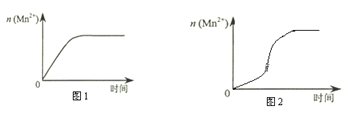
��С��ͬѧ����ļ�����___________________________________________________��
��3����Ѫ�Ƶĺ���ʱ����������ʵ�飺
�ٿɽ�4mLѪҺ������ˮϡ�ͺ������м������������(NH4)2C2O4���壬��Ӧ����CaC2O4��������������ϡ���ᴦ����H2C2O4��Һ��
�ڽ��ٵõ���H2C2O4��Һ����������KMnO4��Һ�ζ�����������ΪCO2����ԭ����ΪMn2+��
���յ�ʱ��ȥ20mL l.0��l0-4mol/L��KMnO4��Һ��
�ζ��յ��������_________________________________��
�����в����ᵼ�²ⶨ���ƫ�͵���______��
A����ƿ�ô��������Һ��ϴ
B���ζ������У���ƿҡ����̫���ң���ƿ����Һ�ν���
C����ʽ�ζ��ܼ��첿���ڵζ�ǰû�����ݣ��ζ��յ�ʱ��������
D���ﵽ�ζ��յ�ʱ�����Ӷ���
���㣺ѪҺ�к������ӵ�Ũ��Ϊ______mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ֿɳ���-���������ͼ��ʾ������طŵ�ʱ��O2��Li+�ڶ��̼���ϵ缫������Li2O2-x��x=0��1��������˵����ȷ����

A. �ŵ�ʱ�����̼���ϵ缫Ϊ����
B. �ŵ�ʱ�����·�����ɶ��̼���ϵ缫����﮵缫
C. ���ʱ���������Һ��Li+����̼������Ǩ��
D. ���ʱ������ܷ�ӦΪLi2O2-x=2Li+��1��![]() ��O2
��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A.��̼����ƣ�aq���м��������������أ�aq����Ca2+��2HCO3����2OH����CaCO3����2H2O��CO32��
B.�Ȼ����������������Ũ��Һ��ϣ�OH- + NH4+=H2O + NH3��
C.ʵ������Cl2��MnO2+4HCl��Ũ��![]() Mn2�� +2Cl- +Cl2��+2H2O
Mn2�� +2Cl- +Cl2��+2H2O
D.������ˮ��Ӧ��Cl2��H2O ![]() 2H����Cl����ClO��
2H����Cl����ClO��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ���������ˮ���ص��ǣ� ��
A.����������ˮ��B.NaCl������ζƷ
C.ʵ��������FeCl3��Һʱ��������D.��TiCl4�Ʊ����ײ���TiO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com