
【题目】25℃时,进行下图所示滴定并得到对应曲线。下列说法错误的是( )

A.Ka2(H2C2O4)=10-4.19
B.直线Ⅰ中X=![]()
C.在NaHC2O4溶液中c(H2C2O4)+c(H+)=c(OH-)+c(C2O42-)
D.Ⅰ、Ⅱ两条直线的斜率均为1
【答案】B
【解析】
H2C2O4溶液中滴入NaOH溶液,先发生反应:H2C2O4+OH-=HC2O4-+H2O,随着碱的不断滴入,溶液的pH不断增大;当H2C2O4完全反应后,HC2O4-与NaOH发生反应HC2O4-+OH-=C2O42-+H2O,所以直线Ⅰ为X=![]() ,直线Ⅱ为X=
,直线Ⅱ为X=![]() 。
。
A. 在pH=4.19点,Ka2(H2C2O4)=![]() =10-4.19,A正确;
=10-4.19,A正确;
B. 由以上分析可知,直线Ⅱ中X=![]() ,B错误;
,B错误;
C. 在NaHC2O4溶液中,HC2O4-![]() C2O42-+H+,HC2O4-+H2O
C2O42-+H+,HC2O4-+H2O![]() H2C2O4+OH-,H2O
H2C2O4+OH-,H2O![]() H++OH-
H++OH-
由水电离出的c(OH-)=c(H+),则溶液中c(H+)-c(C2O42-)=c(OH-)-c(H2C2O4),从而得出c(H2C2O4)+c(H+)=c(OH-)+c(C2O42-),C正确;
D. 直线Ⅰ,lg X=0时,pH=1.22,pH=0时,lg X=1.22(由平衡常数进行计算),从而得出其斜率为1;采用同样的方法,可求出直线Ⅱ的斜率为1,D正确;
故选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是
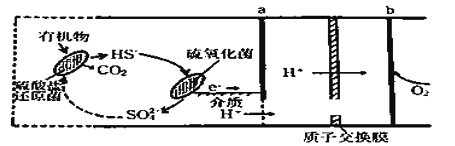
A. HS-在硫氧化菌作用下转化为SO42-的反应为:HS-+4H2O-8e-== SO42-+9H+
B. 电子从b流出,经外电路流向a
C. 如果将反应物直接燃烧,能量的利用率不会变化
D. 若该电池电路中有0.4mol电子发生转移,则有0.45molH+通过质子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:① C(s) + O2(g)=CO2(g) H=-393.5 kJmol-1
②2CO(g) + O2(g)=2CO2(g) H=-566 kJmol-1
③TiO2(s) + 2Cl2(g)=TiCl4(s) + O2(g) H=+141 kJmol-1
则TiO2(s) + 2Cl2(g) + 2C(s)=TiCl4(s) + 2CO(g)的H=_________________。
(2)氯化银在水中存在沉淀溶解平衡AgCl(s)![]() Ag+(aq) + Cl-(aq)。25℃时,氯化银的Ksp=1.8×10-10,现将足量的氯化银加入到0.1 molL-1氯化铝溶液中,银离子浓度最大可达到_____________molL-1。
Ag+(aq) + Cl-(aq)。25℃时,氯化银的Ksp=1.8×10-10,现将足量的氯化银加入到0.1 molL-1氯化铝溶液中,银离子浓度最大可达到_____________molL-1。
(3)20 ℃时,0.1 molL-1 NH4Al(SO4)2溶液的pH=3,则:2c(SO42-)-c(NH4+)-3c(Al3+)≈______________molL-1(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.芳香烃是分子组成符合CnH2n-6(n≥6)的一类物质
B.苯和浓硝酸在55~60℃,浓硫酸存在时发生硝化反应
C.甲苯可以和浓硝酸与浓硫酸的混合物发生硝化反应
D.等质量的烃(CxHy)耗氧量取决于![]() 的值,越大则耗氧多
的值,越大则耗氧多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某同学设计的验证原电池和电解池的实验装置,下列有关说法不正确的是( )
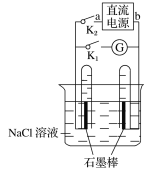
A. 关闭K2、打开K1,试管内两极都有气泡产生
B. 关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多,则a为负极,b为正极
C. 关闭K2,打开K1,一段时间后,用拇指堵住试管移出烧杯,向试管内滴入酚酞,发现左侧试管内溶液变红色,则a为负极,b为正极
D. 关闭K2,打开K1,一段时间后,再关闭K1,打开K2,检流计指针不会偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲酸和苯甲醇(在水中溶解度不大,易溶于有机溶剂,密度约等于水的密度)。反应原理如下:
2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa
C6H5COONa+HCl→C6H5COOH+NaCl
相关物质物理性质如表:
苯甲醛 | 苯甲醇 | 苯甲酸. | 苯 | |
沸点/℃ | 178 | 205 | 249 | 80 |
熔点/℃ | 26 | -15 | 122 | 5.5 |
苯甲酸在水中的溶解 | ||
17℃ | 25℃ | 100℃ |
0.21g | 0.34g | 5.9g |
实验流程如下:

(1)操作①需连续加热1小时(如图1),其中加热固定装置未画出。

仪器A的名称为___,若将仪器B改为图2中的仪器C,效果不如B,请说明原因___。
(2)操作②有关分液漏斗的使用不正确的是___(填字母)。
A.分液漏斗在使用之前必须检查是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时待下层液体放完后立即关闭旋塞,换一个烧杯再打开旋塞使上层液体流下
(3)操作③是用沸水浴加热蒸馏,再进行操作④(如图2),收集___℃的馏分。图2中有一处明显错误,正确的应改为___。
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体;用___冲洗杯壁上残留的晶体。抽滤完成后用少量冰水对晶体进行洗涤,洗涤前应先___。
(5)用电子天平准确称取0.2440g苯甲酸于锥形瓶中加100mL蒸馏水溶解(必要时可以加热),再用0.1000mol·L-1的标准氢氧化钠溶液滴定,共消耗标准氢氧化钠溶液19.20mL,苯甲酸的纯度为___%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 H2(g) + Cl2 (g)===2HCl(g) Δ H =- 184.6 kJ · mol-1则反应:HCl(g)===1/2H2(g)+1/2Cl2(g)的ΔH 为( )
A.+184.6 kJ·mol-1B.-92.3 kJ·mol-1
C.-369.2 kJ·mol-1D.+92.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中,有广泛应用,它的工作原理如下:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2.下列叙述正确的是
Cd(OH)2+2Ni(OH)2.下列叙述正确的是
A. 该电池放电的时候,负极附近pH增大
B. 放电时每转移2mol电子,有2mol NiO(OH)被氧化
C. 充电时,阳极反应式是Ni(OH)2-e-+OH-=NiO(OH)+H2O
D. 充电时,Cd电极接电源正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com