

| A、将电能转换为化学能 |
| B、电子由锌片流出 |
| C、银片为电池的负极 |
| D、电池反应为:Cu+2AgNO3═Cu(NO3)2+2Ag |
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
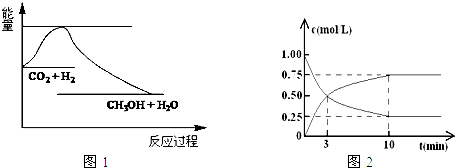
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解水制取氢气是理想而经济的制氢方法 |
| B、发展氢燃料电池汽车不需要安全高效的储氢技术 |
| C、氢燃料电池汽车的使用可以有效减少城市空气污染 |
| D、氢燃料电池把氢气和氧气燃烧放出的热能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、前者大于后者 |
| B、前者小于后者 |
| C、前者等于后者 |
| D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡正向移动 |
| B、平衡不移动 |
| C、平衡时B的体积分数增大 |
| D、平衡时C的体积分数可能变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验室为了对配制好的溶液进行精确测定其浓度,一般选用高纯度、性质稳定、相对分子质量较大的物质做为基准物进行标定 |
| B、化学实验要注意控制条件,考虑反应物的浓度和用量,选择适宜的温度范围,以及是否要使用催化剂等 |
| C、倾析法适用于分离或洗涤结晶颗粒较大、静置后容易沉降至容器底部的沉淀 |
| D、火柴头的药粉中含有对空气敏感的易燃物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+,Na+,SO42-,NO3- |
| B、Ba2+,NH4+,OH-,MnO4- |
| C、H+,K+,Cl-,CO32- |
| D、Na+,Fe2+,NO3-,OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com