
| A、实验室为了对配制好的溶液进行精确测定其浓度,一般选用高纯度、性质稳定、相对分子质量较大的物质做为基准物进行标定 |
| B、化学实验要注意控制条件,考虑反应物的浓度和用量,选择适宜的温度范围,以及是否要使用催化剂等 |
| C、倾析法适用于分离或洗涤结晶颗粒较大、静置后容易沉降至容器底部的沉淀 |
| D、火柴头的药粉中含有对空气敏感的易燃物质 |


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、将电能转换为化学能 |
| B、电子由锌片流出 |
| C、银片为电池的负极 |
| D、电池反应为:Cu+2AgNO3═Cu(NO3)2+2Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、64.7% |
| B、47.5% |
| C、32.2% |
| D、28.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高氯酸的酸性比亚硫酸强 |
| B、次氯酸的氧化性比稀硫酸强 |
| C、氯化氢比硫化氢的热稳定性好 |
| D、氯原子最外层电子数比硫原子多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
239 94 |
| A、239 | B、145 |
| C、94 | D、51 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KOH的摩尔质量是56g |
| B、一个碳原子的质量就是其相对原子质量 |
| C、硫原子的质量就是硫的相对原子质量 |
| D、氮气的摩尔质量在数值上等于它的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
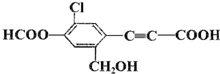 ,关于该有机物描述正确的是( )
,关于该有机物描述正确的是( )| A、该有机物分子式为:C11H5O5Cl |
| B、分子中最多有9个碳原子共平面 |
| C、1mol 该有机物分别与Na、NaOH、NaHCO3完全反应,消耗Na、NaOH、NaHCO3的物质的量依次为:2mol、5mol、1mol |
| D、该有机物不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑩ | |||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | ⑨ | ||
| 4 | ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com