
【题目】请分析细胞内4种重要有机物的组成及功能,回答下列问题:
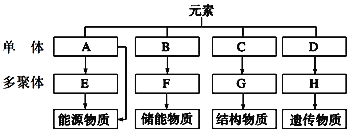
(1)A一般是指________;E在动物细胞中是指____________,在植物细胞中主要是________。
(2)F是指__________,除此之外,脂质还包括__________和固醇。
(3)C是指__________,由m个C构成G物质时,其相对分子质量最多可减少____________。
(4)D是指____________,生物体内的H分为________和________两大类。(写中文名称)
(5)四大有机物都含有的化学元素是______________。
【答案】 葡萄糖 糖原 淀粉 脂肪 磷脂 氨基酸 18(m-1) 核苷酸 核糖核酸 脱氧核糖核酸 C、H、O
【解析】试题分析:根据不同化合的功能可以推断,糖类是的能源物,因此E示多糖,其单体A为葡萄糖;脂肪是要的储能物质,因此F为脂肪,B为甘油和脂肪酸;蛋白质是重要的结构物质,所以G是蛋质,其单体C是氨基酸;核酸是遗传物质,因此H是核酸,其单体D是核苷酸。
(1)因为糖类是主要的能源物质,因此E表示多糖,A为葡萄糖。动物体内的多糖为糖原;植物体的多糖包括淀粉和纤维素,因为纤维素不能提供能量,不属于能源物质,因此植物中的E主要指淀粉。
(2)脂肪是主要的储能物质,因此F是脂肪,脂肪属于脂质的一种,脂质还包括磷脂和固醇。
(3)蛋白质是重要的结构物质,因此G是蛋白质,C是氨基酸。根据相邻两个氨基酸脱出1分子水形成一个肽键,分子质量减少18,一条肽链脱出的水分子为氨基酸数-1。计算由m个氨基酸构成蛋白质时,其相对分子质量最多可减少18(m-1)。
(4)核酸是遗传物质,因此H是核酸,D为核苷酸。生物体内核酸分为两种,DNA和RNA。
(5) 糖类是由C、H、O元素组成;蛋白质是由C、H、O、N元素构成,有些含有P、S;脂质是由C、H、O元素构成,有些含有N、P;核酸是由C、H、O、N、P元素构成;所以四大有机物都含有的化学元素是C、H、O。


科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= , 已知:K(300℃)>K(350℃),该反应是反应(填“放热”或“吸热”).
(2)图中表示NO2的变化的曲线是 , 用O2的浓度变化表示从0~2s内该反应的平均速率v=
(3)能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0L恒容密闭容器中充入2mol SO2和1mol O2 , 发生反应:2SO2(g)+O2(g)2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A.反应在前2 s 的平均速率v(O2)=0.4 molL﹣1s﹣1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3 , 达到平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2 , 反应达到新平衡时n(SO3)/n(O2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表述正确的是( ) ①常温时pH=11的KOH溶液与pH=3的醋酸等体积混合,所得溶液pH<7
②二氧化硅是酸性氧化物,但它能与某种酸反应
③Fe2O3(s)+3H2(g)═ 2Fe(s)+3H2O(g)△H>0,△S>0任何条件下都不能自发进行
④丁达尔效应可用于区别溶液和胶体,电泳现象能证明胶体带电荷
⑤钢铁的吸氧腐蚀,正极发生反应:O2+4e﹣+4H+═2H2O
⑥H2的燃烧热为285.8kJ/mol,则表示H2的燃烧热的热化学方程式为H2(g)+ ![]() O2(g)═ H2O(g)△H=﹣285.8kJ/mol.
O2(g)═ H2O(g)△H=﹣285.8kJ/mol.
A.①④
B.①②
C.④⑥
D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应都有沉淀生成,其中属于氧化还原反应的是( )
A. Na2SO4+BaCl2=2NaCl+BaSO4↓B. 4Fe(OH)2+O2+2H2O= 4Fe(OH)3↓
C. FeCl3+3KOH=Fe(OH)3↓+3KClD. CuCl2+2NaOH=Cu(OH)2↓+2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.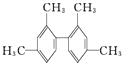 分子中至少有10个碳原子处于同一平面
分子中至少有10个碳原子处于同一平面
B.蛋白质和油脂都属于高分子化合物,一定条件下能水解
C.等物质的量的苯和苯甲酸完全燃烧消耗的氧气的量不相等
D.经测定乙二醇和苯组成的混合物中氧的质量分数为8%,则此混合物中碳的质量分数是84%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)2NO2(g)△H=+57kJmol﹣1 , 在温度为T时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的为( ) 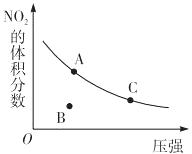
A.A,C两点的反应速率:v(A)>v(C)
B.A,C两点气体的颜色:A深,C浅
C.B点正逆反应速率:v(正)>v(逆)
D.A,C两点气休的平均相对分子质量:A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A.H2O(g)=H2(g)+ ![]() O2(g);△H=+242kJmol﹣1
O2(g);△H=+242kJmol﹣1
B.2H2(g)+O2(g)+2H2O(l);△H=﹣484kJmol﹣1
C.H2(g)+ ![]() O2(g)=H2O(g);△H=+242kJmol﹣1
O2(g)=H2O(g);△H=+242kJmol﹣1
D.2H2(g)+O2(g)=2H2O(g);△H=﹣484kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时沉淀的物质的量y mol与加入NaOH溶液和盐酸的体积x mL的关系图,根据图示判断,下列结论中不正确的是

A. N点时溶液中的溶质只有NaCl
B. 原混合溶液中c (MgCl2)∶c (AlCl3)=1∶2
C. c (NaOH)=c (HCl)
D. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
【答案】B
【解析】由图象可知N→M发生Al(OH)3+OH-===AlO2-+2H2O,设氢氧化钠溶液浓度为c,则消耗氢氧化钠0.01cmol,n[Al(OH)3]=n(AlCl3)=0.01cmol;ON消耗氢氧化钠0.05cmol,分别发生MgCl2+2NaOH=Mg(OH)2↓+2NaCl、AlCl3+3NaOH=Al(OH)3↓+3NaCl,可知n(MgCl2)=(0.05cmol-0.01c×3mol)/2=0.01cmol,则c(AlCl3):c(MgCl2)=1:1,M点时溶液成分为NaAlO2,之后继续加入溶液后沉淀质量逐渐增大,此时应加入盐酸,发生反应为:NaAlO2+HCl+H2O= Al(OH)3↓+NaCl,继续加入盐酸沉淀逐渐溶解,生成氯化镁、氯化铝和氯化钠,则消耗的氢氧化钠和HCl的物质的量相等,A.根据分析可知,N点时溶液中的溶质只有NaCl,A正确;B.原混合溶液中c(MgCl2):c(AlCl3)=1:1,B错误;C.由横坐标可知消耗盐酸和氢氧化钠的体积相同,则二者物质的量浓度相同,C正确;D.根据分析可知,M点之前加入的是NaOH溶液,M点之后加入的是盐酸,D正确;答案选B。
【题型】单选题
【结束】
16
【题目】证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是
①先滴加氯水,再滴加KSCN溶液后显红色
②先滴加KSCN溶液,不显红色,再滴加氯水后显红色
③滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后呈红褐色
④只需滴加KSCN溶液
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com