
����Ŀ��һ���¶�ʱ����2.0L�����ܱ������г���2mol SO2��1mol O2 �� ������Ӧ��2SO2��g��+O2��g��2SO3��g��������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 2 | 4 | 6 | 8 |
n��SO3��/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
����˵����ȷ���ǣ� ��
A.��Ӧ��ǰ2 s ��ƽ������v��O2��=0.4 molL��1s��1
B.���������������䣬���ѹ����1.0 L��ƽ�ⳣ��������
C.��ͬ�¶��£���ʼʱ�������г���4 mol SO3 �� �ﵽƽ��ʱ��SO3��ת���ʴ���10%
D.�����¶Ȳ��䣬����������ٳ���2 mol SO2��1 mol O2 �� ��Ӧ�ﵽ��ƽ��ʱn��SO3��/n��O2������
���𰸡�D
���������⣺A�����ݱ���������֪����n��SO3��=1.8mol���÷�Ӧ�ﵽƽ��״̬����Ӧ��ǰ2s��ƽ������v��SO3��= ![]() =0.2molL��1s��1 �� ͬһ���淴Ӧ��ͬһ��ʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�v��O2��=
=0.2molL��1s��1 �� ͬһ���淴Ӧ��ͬһ��ʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�v��O2��= ![]() ��0.2molL��1s��1=0.1molL��1s��1 �� ��A����B����ѧƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬��ѧƽ�ⳣ�����䣬��ѹǿ������Ũ�ȶ��أ���B����
��0.2molL��1s��1=0.1molL��1s��1 �� ��A����B����ѧƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬��ѧƽ�ⳣ�����䣬��ѹǿ������Ũ�ȶ��أ���B����
C����ͬ�¶��£���ʼʱ�������г���4mol SO3 �� �������������ȫת��Ϊ���������������������������������ʵ����ֱ���4mol��2mol��Ϊԭ����2��������ѹǿƽ�������ƶ������������ת�����������Զ�������ת���ʴ���90%����ͬ�¶��£���ʼʱ�������г���4mol SO3 �� �ﵽƽ��ʱ��SO3��ת����С��10%����C����
D���¶Ȳ��䣬����������ٳ���2mol SO2��1mol O2 �� ������ѹǿ��ƽ�������ƶ���������������ʵ������ӣ����������ʵ�����С�����Ա�ֵ����D��ȷ��
��ѡD��
�����㾫����������Ĺؼ��������⻯ѧƽ��ļ�������֪ʶ�����շ�Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���췯�ƣ��ظ����ƣ�Na2Cr2O7��2H2O������Ҫ�Ļ�������ԭ�ϣ���ӡȾ��ҵ����ƹ�ҵ��Ƥ�﹤ҵ�����������ڻ�ѧ��ҵ����ҩ��ҵ��Ҳ������������Ӧ������ʮ�ֹ㷺��
ʵ�����к췯�ƿ��ø�������Ҫ�ɷ֣�FeO��Cr2O3���������¹�������ȡ��
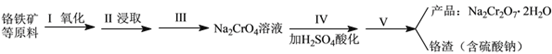
��1������I�з�Ӧ�Ļ�ѧ����ʽΪ��4FeO��Cr2O3(s)+8Na2CO3(s)+7O2 (g)![]() 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ��H<0�÷�Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽΪ__________________________��
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ��H<0�÷�Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽΪ__________________________��
��2���ڳ����¸÷�Ӧ�ٶȼ��������д�ʩ����ʹ��Ӧ�����������_____________________________ ��
a�������¶� b����ʱת������CO2 c����ԭ�Ϸ��� d�����Ӵ��������
��3����������������Һ�Լ��ԣ����г�����Na2CrO4�����������Ԫ�ص������������ǵĻ�ѧʽ������__________________________��____________________________��
��4���������轫��Һ��pH����7~8����У���Ŀ����_____________________________________��
��5���������ữʱ��CrO42��ת��ΪCr2O72����д��ƽ��ת�������ӷ���ʽ��_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A.�������еμӰ�ˮ��H++OH���TH2O
B.Fe��OH��3��������Fe��OH��3+3H+�TFe3++3H2O
C.��Na2S2O3��Һ��ͨ������������S2O ![]() +2Cl2+3H2O�T2SO
+2Cl2+3H2O�T2SO ![]() +4Cl��+6H+
+4Cl��+6H+
D.ͭ����ϡ���3Cu+8H++2NO ![]() �T3Cu2++2 NO��+4H2O
�T3Cu2++2 NO��+4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����20����������������Ϊδ���Ķ���ȼ������Դ���о������Ѹ�ٷ�չ�����һ��������һ����Ҫ����������Դ��ʯ�͡�ú��ԭ���ܵȵ���������ȡ����ν��������Դ��������������Ȼ��Ŀ����ṩ�ֳ���ʽ��������Դ��Ϊһ����Դ����ú��ʯ�͡�̫���ܺ�ԭ���ܵȣ�
��1��Ϊ����Ч��չ��������Դ�����ȱ����Ƶ����۵����������пɹ������ֽϾ�������Դ�ɳ������õ��������ķ�����
A.���ˮ
B.п��ϡ���ᷴӦ
C.��⺣ˮ
D.��ʯ�͡���Ȼ��Ϊԭ��
��2������ȼ��ʱ������С������������֪���Ȼ�ѧ����ʽΪ��
C��s��+O2��g��=CO2��g������H=��393.5kJmo��1L
2H2��g��+O2��g��=2H2O��l������H=��571.6kJmo��1L
��ͨ������˵����������������̼ȼ��ʱ���������ı��� ��
��3������Դ�п���ʵ����Դ�����棬Ҳ�п���ʵ�־��á���Ч�����ͣ��о��������ɽ������⻯��ֳƼ���⻯����������⻯���У���ԭ������ڽ����ľ����϶֮�䣬����ɲ��̶���ͨ���Ƿǻ�ѧ�����ģ��磺LaH2 �� 76��TiH1.73��CeH2.69��ZrH1.98��PrH2.85��TaH0.78 �� ��֪��״���£�1������ٷ۴�Լ������896������������ٷ۵��ܶ�Ϊ10.64g/cm3�����ԭ������Ϊ106.4������д���٣�Pd�����⻯��Ļ�ѧʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ���
A.��������ϼۣ�P��N��CB.��һ�����ܣ�Li��Na��K
C.���ȶ��ԣ�H2O��HF��H2SD.���ԣ�LiOH��NaOH��KOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���� (����)
A.����ֻ�ܼӿ컯ѧ��Ӧ����
B.����Ӱ��ijЩ��ѧ��Ӧ���ʵ��������֮һ
C.������ѧ��Ӧ���ʵ���Ҫ������Ũ��
D.����ʲô��Ӧ������Ũ�ȣ�����ȣ����ѹ�������Լӿ췴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� (����)
A.�Ǽ�����һ����ɫȾ��
B.�Ǽ�����һ�ְ�ɫȾ��
C.�Ǽ������п�ȼ��
D.�Ǽ����п�ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϸ����4����Ҫ�л������ɼ����ܣ��ش��������⣺
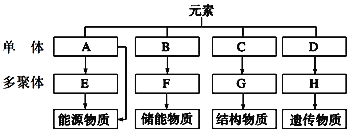
(1)Aһ����ָ________��E�ڶ���ϸ������ָ____________����ֲ��ϸ������Ҫ��________��
(2)F��ָ__________������֮�⣬֬�ʻ�����__________�̴���
(3)C��ָ__________����m��C����G����ʱ������Է����������ɼ���____________��
(4)D��ָ____________���������ڵ�H��Ϊ________��________�����ࡣ��д�������ƣ�
(5)�Ĵ��л��ﶼ���еĻ�ѧԪ����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йع���ϵ�˵������ȷ����( )
A. ����������õİ뵼����Ϻ�����̫���ܵ�صIJ���
B. SiO2������������ά
C. ��ͨ�������Դ��ʯ��ʯ��ʯӢΪԭ�Ͼ������ս���Ƴɵ�
D. SiO2�������������������ˮ���ɹ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com