
【题目】下列离子方程式正确的是( )
A.向盐酸中滴加氨水:H++OH﹣═H2O
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O
C.向Na2S2O3溶液中通入足量氯气:S2O ![]() +2Cl2+3H2O═2SO
+2Cl2+3H2O═2SO ![]() +4Cl﹣+6H+
+4Cl﹣+6H+
D.铜溶于稀硝酸:3Cu+8H++2NO ![]() ═3Cu2++2 NO↑+4H2O
═3Cu2++2 NO↑+4H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】写出下列离子方程式对应的一个化学方程式:
(1)2H+ + CO32— = H2O + CO2↑ (2) 2OH-+ Cu2+ = Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做了如下四组实验:①号试管中豆浆+双缩脲试剂:②号试管中氨基酸溶液+双缩脲试剂:③号试管中淀粉+淀粉酶+双缩脲试剂;④号试管中煮沸后的淀粉酶+双缩脲试剂。四组实验中出现紫色的有
A. 四组B. 三组C. 两组D. 一组
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= , 已知:K(300℃)>K(350℃),该反应是反应(填“放热”或“吸热”).
(2)图中表示NO2的变化的曲线是 , 用O2的浓度变化表示从0~2s内该反应的平均速率v=
(3)能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知98%的浓硫酸的物质的量浓度为18.4mol/L,则49%的硫酸的物质的量浓度 ( )
A. 等于9.2 mo1/L B. 小于 9.2 mo1/L
C. 大于 9.2 mo1/L D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有如下三个热化学方程式:
H2(g)+ ![]() O2(g)═H2O(g)△H=a kJmol﹣1
O2(g)═H2O(g)△H=a kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(l)△H=b kJmol﹣1
O2(g)═H2O(l)△H=b kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H=c kJmol﹣1
关于它们的下列表述正确的是( )
A.它们都是吸热反应
B.a、b和c均为正值
C.a=b
D.2b=c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是中学化学常见的六种单质,原子序数依次增大的短周期主族元素,其中D、E是固体,其余均为气体.图中其他物质均为化合物,六种元素都不在同一主族.
(1)写出下列物质的名称:甲 , 乙 .
(2)写出实验室制取F的化学方程式 , 检验F收集满的方法 .
(3)Y和CuO的反应方程式 .
(4)写出乙和过量CO2反应的离子方程式 .
(5)D和E形成原电池的两个电极,NaOH溶液是电解质溶液.E的一极为原电池的极,该极的电极反应式为 .
(6)73g X与足量的NaOH溶液反应放热Q kJ,写出该反应的热化学方程式 .
(7)D的最高价氧化物对应水化物的Ksp=1.8×10﹣11 , 该物质的溶液中,要使D离子的浓度降至1.8×10﹣9 mol/L,25℃时溶液的pH应调至 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0L恒容密闭容器中充入2mol SO2和1mol O2 , 发生反应:2SO2(g)+O2(g)2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A.反应在前2 s 的平均速率v(O2)=0.4 molL﹣1s﹣1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3 , 达到平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2 , 反应达到新平衡时n(SO3)/n(O2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)2NO2(g)△H=+57kJmol﹣1 , 在温度为T时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的为( ) 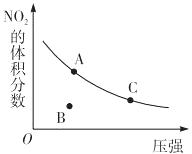
A.A,C两点的反应速率:v(A)>v(C)
B.A,C两点气体的颜色:A深,C浅
C.B点正逆反应速率:v(正)>v(逆)
D.A,C两点气休的平均相对分子质量:A>C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com