
| A�� | �٢ܢ� | B�� | �٢ۢ� | C�� | �٢ڢ� | D�� | �٢ڢۢܢ� |
���� 3SnCl2+12Cl-+2H3AsO3+6H+�T2As+3SnCl62-+6M�е���غ㣬��MΪˮ����Ӧ��SnԪ�ش�+2��������+4�ۣ�AsԪ�ش�+3���½���0�ۣ��Դ������
��� �⣺����ʽ��SnԪ�ش�+2��������+4�ۣ�SnCl2�ǻ�ԭ����SnCl���������AsԪ�ش�+3���½���0�ۣ�H3AsO3����������As�ǻ�ԭ���ClԪ�ػ��ϼ�û�з����仯�������Ƴ���ԭ�ԣ�Cl-��As��ÿ����7.5 g As����ԭ��ʧȥ���ӵ����ʵ���Ϊ$\frac{7.5g}{75g/mol}$��3=0.3 mol�����������غ�͵���غ���֪MӦΪH2O����Ȼ�٢ܢ���ȷ����ѡA��
���� ���⿼��������ԭ��Ӧ��Ϊ�߿���Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ���ע���ԭ���غ㼰���ϼ۽Ƕȷ�������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
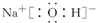 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ̼ | �� | Y | |
| X | �� | Z |
 �����е��Ļ��ϼ�Ϊ��-2��ʵ���ҿ��ô���������Һ�백��Ӧ�Ʊ���������Ӧ�Ļ�ѧ����ʽΪ��NaClO+2NH3=N2H4+NaCl+H2O ��
�����е��Ļ��ϼ�Ϊ��-2��ʵ���ҿ��ô���������Һ�백��Ӧ�Ʊ���������Ӧ�Ļ�ѧ����ʽΪ��NaClO+2NH3=N2H4+NaCl+H2O ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ȴ����俪ˮ | B�� | �ȴ���ʳ��ˮ | ||
| C�� | �ȴ���ţ�� | D�� | ע�����������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol H2���6.02��1023��H | B�� | 1 mol������6.02��1023��O2 | ||
| C�� | 1 mol CaCl2��Һ�ﺬ��1 mol���� | D�� | 1 mol H+�к���H+��ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2 | B�� | NH3 | C�� | H2O | D�� | SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2O3 �ǻ�ԭ�� | B�� | CO�������� | ||
| C�� | �������õ�6mol���� | D�� | ��ԭ��ʧȥ8mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ԣ�A��=0.5mol•L-1•S-1 | B�� | �ԣ�B��=0.3 mol•L-1•S-1 | ||
| C�� | �ԣ�C��=0.8mol•L-1•S-1 | D�� | �ԣ�D��=1 mol•L-1•S-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com