
【题目】已知乙烯在一定条件下能发生下列转化,回答下列问题:

(1)反应①的反应类型是__________;物质C中所含官能团的名称是__________。
(2)分别写出②、④反应的化学方程式(有机物用结构简式表示):__________、__________。
(3)实验室制取乙酸乙酯的装置如下图所示。能完成本实验的装置是__________(填“甲”、“乙”或“丙”),试管B内盛放的液体是__________。

【答案】 加成反应 羧基 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3CH2OH+CH3COOH
2CH3CHO+2H2O CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O 乙、丙 饱和碳酸钠溶液
CH3COOCH2CH3+H2O 乙、丙 饱和碳酸钠溶液
【解析】乙烯经过反应得到A,A经过两步反应得到C,而A和C可生成乙酸乙酯,因此A为乙醇,B为乙醛,C为乙酸。乙烯与水发生加成反应生成乙醇,乙醇氧化生成乙醛,乙醛进一步氧化生成乙酸。
(1)应①为乙烯与水发生加成反应生成乙醇;经推断可知C为乙酸,乙酸中所含官能团是羧基;(2)反应②为乙醇的催化氧化过程,方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;反应④为乙醇与乙酸发生酯化反应,方程式为CH3CH2OH+CH3COOH
2CH3CHO+2H2O;反应④为乙醇与乙酸发生酯化反应,方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;(3)制取乙酸乙酯时,蒸汽中往往含有乙醇和乙酸,所以用饱和碳酸钠溶液吸收掉从而与乙酸乙酯分离,但是二者易溶于水而产生倒吸,乙导管没有插入到液面以下,丙导管上端容积较大,二者都可防止倒吸。
CH3COOCH2CH3+H2O;(3)制取乙酸乙酯时,蒸汽中往往含有乙醇和乙酸,所以用饱和碳酸钠溶液吸收掉从而与乙酸乙酯分离,但是二者易溶于水而产生倒吸,乙导管没有插入到液面以下,丙导管上端容积较大,二者都可防止倒吸。


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】氧、硫位于元素周期表的 VIA 族,其化合物在化工生产中有广泛应用。
(1)CuSO4可由 Cu+H2SO4+H2O2=CuSO4+2H2O 反应制得,该反应应要控制在 40—50℃,原因是________________________________________________。
(2)蛋白质中也含有硫元素,为了测定硫元素质量分数,取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2S2O32-+I2=S4O62-+2I-
① 滴定终点的现象为:________________________________________。
② 取蛋白质样品 mg 进行测定,采用 C1mol/L 的碘水 V1mL 进行吸收,滴定过量的碘时消耗 C2mol/L 硫代硫酸钠溶液 V2mL。该蛋白质中的硫元素的质量分数为______________。
③ 若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值___(填“偏大”或“偏小”或“无影响”)。
(3)苯硫酚(C6H5SH)是一种用途广泛的有机合成中间体。工业上用常用氯苯(C6H5Cl)和硫化氢(H2S)为主要原料制备苯硫酚,但会有副产物苯( C6H6)生成。
I:C6H5Cl(g)+H2S(g) C6H5SH(g)+HCl(g) △H1=-16.8kJ/mol
II:C6H5Cl(g)+H2S(g)===C6H6(g)+ HCl(g)+1/8S8(g) △H2
反应 II 的焓变不易测量,现查表得如下数据:
III: C6H5SH(g)=== C6H6(g)+1/8 S8(g) △H3=-29.0kJ/mol
④ △H2= __________________________
现将一定量的氯苯和硫化氢置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20分钟测定生成物的浓度,得到图二。
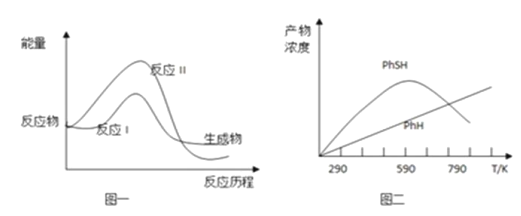
⑤ 上述反应 I、II 的能量变化如图一所示,则在相同条件下,反应速度 v(I)___ v( II)(填写“>”,“<”,“=”)。
⑥ 图二可知,790℃时所测生成物苯硫酚浓度减小,原因为_________
A.温度升高,平衡逆向移动 B.反应Ⅱ温度升高反应速率加快
⑦ 590℃时,2mol 氯苯和 5mol 硫化氢混合气体在 VL 的固定容积中进行反应 I 和II,达到平衡时,测得容器中苯硫酚的物质的量为 1mol,苯的物质的量为0.5mol,则该温度下反应 I 的平衡常数为_______。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是中学化学重要的非金属元素之一,请回答下列有关问题。
已知:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6kJ/mol
2SO3(g) △H=-196.6kJ/mol
2NO(g)+O2(g)![]() 2NO2(g) △H=-113.0kJ/mol
2NO2(g) △H=-113.0kJ/mol
(1)反应NO2(g)+ SO2(g)![]() SO3(g)+NO(g)的ΔH= ______kJ/mol 。
SO3(g)+NO(g)的ΔH= ______kJ/mol 。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 _________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO2的同时消耗1 molNO
(3)S2Cl2和SCl2均为重要的工业化合物。已知:
a.S2(l)+Cl2(g)![]() S2Cl2(g) △H1
S2Cl2(g) △H1
b.S2Cl2(g)+ Cl2(g)![]() 2SCl2(g) △H2
2SCl2(g) △H2
—定压强下,向10 L密闭容器中充入1 molS2Cl2和1 mol Cl2,发生反应b。Cl2与SCl2的消耗速率(υ)与温度(T)的关系如图所示:
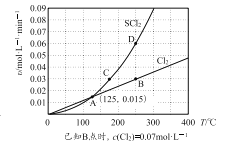
① A、B、C、D四点对应状态下,达到平衡状态的有______(填字母),理由是_______。
②—定温度下,在恒容密闭容器中发生反应a和反应b,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________(填“增大”或“减小”或“不变”),理由是________。
II.氮有不同价态的化合物,如氨、氮气、亚硝酸钠、乙二胺等。
图(I)和图(II)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。
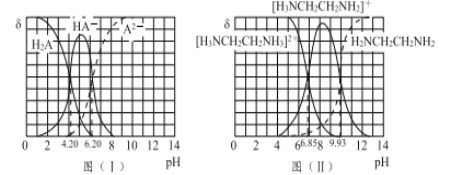
(1)H3NCH2CH2NH3A溶液显____(填“酸”或“碱”)性。
(2)乙二胺在水溶液中发生第二步电离的方程式:____________________,其平衡常数Kb2= _______________________ 。
(3)向20 mL 0.1 mol/L的H2A溶液加入10 mL 0.1 mol/L H2NCH2CH2NH2溶液后,溶液中各离子浓度大小的关系为 ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某食用香料乙酸橙花酯的结构简式如图所示,关于该有机物的下列叙述中正确的是( )
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③它的同分异构体中有芳香族化合物
④1mol该有机物水解时只能消耗1molNaOH
⑤1mol该有机物在一定条件下能和3mol H2反应.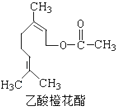
A.①②③
B.①②④
C.①②⑤
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸在一定条件下所形成的聚酯的结构简式为 ![]() ,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )
,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )
A.降解塑料是一种纯净物
B.其生产过程中的聚合方式与聚苯乙烯相似
C.它属于一种线型高分子材料
D.其相对分子质量为72
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的a~g元素,回答下列问题:
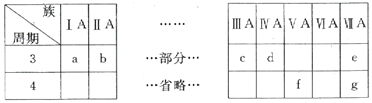
(1)d元素位于金属与非金属的分界线处,常用作__________材料。
(2)f的元素符号为As,其最高价氧化物的化学式为__________。
(3)a、b、c三种元素的最高价氧化物对应水化物的碱性逐渐减弱,试从原子结构的角度解释上述变化规律__________。
(4)e元素的非金属性强于g,请写出一个离子方程式证明:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
(1)D分子中官能团的名称是 , 高分子化合物E的名称是;
(2)反应②的化学方程式是;反应④的化学方程式是 .
(3)某同学用如图2所示的实验装置制取少量乙酸乙酯.实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲中的导管不伸入液面下的原因是;
②上述实验中饱和碳酸钠溶液的作用是;
③在实验室利用B和D制备乙酸乙酯的实验中,若用1mol B和1mol D充分反应,不能生成1mol 乙酸乙酯,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备下列物质时,不用加入浓H2SO4的是( )
A. 由苯制取硝基苯 B. 用乙酸和乙醇制备乙酸乙酯
C. 由1,2-二溴乙烷制乙二醇 D. 由乙醇制乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )

A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q)
C. 离子Y2-和Z3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com