
【题目】选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( ) 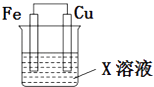
A.6种
B.5种
C.4种
D.3种
科目:高中化学 来源: 题型:
【题目】科学家在利用无土栽培法培养一些名贵花卉时,培养液中添加了多种必需的化学元素,其配方如下表:
离子 | K+ | Na+ | Mg2+ | Ca2+ | N03- | H2PO3- | SO42- | Zn2+ |
培养液浓度(mol/L) | 1 | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
其中植物根细胞吸收量最少的离子是
A. N03- B. SO42- C. Zn2+ D. H2PO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中数据合理的是 ( )
A.用10 mL 量筒量取5.2 mL盐酸
B.用pH试纸测得某溶液的pH值为12.5
C.用托盘天平称取25.12gNaCl固体
D.用100 mL容量瓶配制150mL0.1 mol/L的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现:
①Si(s) +3HCl(g)![]() SiHCl3(g) + H2(g) △H= -381kJ/mol
SiHCl3(g) + H2(g) △H= -381kJ/mol
②SiHCl3(g)+H2(g)![]() S(s) + 3HCl(g)
S(s) + 3HCl(g)
对上述两个反应的下列叙述中,不正确的是
A. 两个反应都是置换反应 B. 反应②是吸热反应
C. 两个反应互为可逆反应 D. 两个反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的分离方法不正确的是 ( )
A.用酒精萃取碘水中的碘B.用淘洗的方法从沙里淘金
C.用蒸馏的方法将自来水制成蒸馏水D.用过滤的方法除去食盐水中的泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是已知: ①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)( )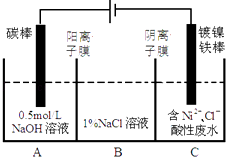
A.碳棒上发生的电极反应:4OH﹣﹣4e﹣═O2↑+2H2O
B.为了提高Ni的产率,电解过程中需要控制废水pH
C.电解过程中,B中NaCl溶液的物质的量浓度将不断减小
D.若将图中阳离子膜去掉,将
A.B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉和纤维素是常见的多糖,在一定条件下它们都可以水解生成葡萄糖。
(1)淀粉在浓硫酸作用下水解生成葡萄糖的化学方程式为___________。
(2)某学生设计了如下实验方案用以检验淀粉水解的情况:
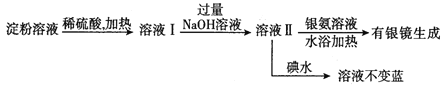
下列结论正确的是_______。
A.淀粉尚有部分未水解 B.淀粉已完全水解
C.淀粉没有水解 D.淀粉已水解,但不知是否完全水解
(3)一种测定饮料中糖类物质含量(所有糖类物质以葡葡糖计算)的方法如下:
取某无色饮料20.00mL加入稀硫酸煮沸,充分反应后,冷却,加入适量的氢氧化钠溶液并稀释至100.00mL。取10.00mL稀释液,加入30.00mL0.0150mol/L标准溶液,置于暗处15分钟。然后滴加2~3滴淀粉溶液作指示剂,再用0.01200mol/LNa2S2O3标准溶液滴定反应所剩余的I2,当溶液由蓝色变为无色且半分钟不变时,反应达到终点,共消耗Na2S2O3标推溶液25.00mL。己知:
a.I2在碱性条件下能与萄萄糖反应:C6H12O6+I2+3NaOH=C6H11O7Na+2NaI+2H2O
b. Na2S2O3与I2能发牛如下反应:I2+2Na2S2O3=2NaI+Na2S4O6
①配制100.00mL0.01500mol/LI2标准溶液,所必需的玻璃仪器有烧杯、玻璃棒、胶头滴管和____。
②向饮料中加入稀硫酸并充分煮沸的目的是___________。
③计算该饮料中糖类物质的含量(单位mg/mL)(写出计算过程)。______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大火炬燃料是丙烯(C3H6)
(1)丙烷脱氢可得丙烯.已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJmol﹣1CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJmol﹣1 则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的△H=kJmol﹣1
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2 , 负极通入丙烷,电解质是熔融碳酸盐.电池总反应方程式为;放电时,CO32﹣移向电池的(填“正”或“负”)极.
(3)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10﹣5 molL﹣1 . 若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3﹣+H+的平衡常数K1= . (已知:10﹣5.60=2.5×10﹣6)
HCO3﹣+H+的平衡常数K1= . (已知:10﹣5.60=2.5×10﹣6)
(4)常温下,0.1molL﹣1NaHCO3溶液的pH大于8,则溶液c(H2CO3)c(CO32﹣)(填“>”、“=”或“<”),原因是(用离子方程式和文字说明)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com