
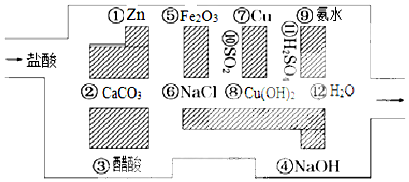
分析 (1)解决该题应该找出一条不能和盐酸发生反应的物质构成的路.酸的化学性质有:能够和酸碱指示剂变色,能够和活泼金属反应,能够和金属氧化物反应,能够和碱反应,能够和某些盐反应.活泼金属即在金属活动性顺序表中氢前的金属,酸和金属氧化物、碱、盐发生的反应是复分解反应;
(2)在能和盐酸反应的物质中,NaOH、Cu(OH)2和氨水为碱,据此写出化学方程式;
(3)在水溶液中和熔融状态下均不能导电的化合物为非电解质,包括蔗糖、酒精、非金属氧化物和氨气等;
(4)CaCO3是强电解质,能完全电离为钙离子和碳酸根;
(5)CaCO3是弱酸盐,能和盐酸发生复分解反应;
(6)一个化学方程式能拆出的Ag++Cl-=AgCl↓形式,说明是可溶性银盐和盐酸或可溶性盐酸盐反应,生成氯化银和一种强酸或可溶性盐,据此分析.
解答 解:(1)利用图示的物质对相关的与盐酸不能反应的物质作出判断即可,由于盐酸不能和③醋酸、⑥NaCl、⑩SO2、⑦Cu、⑪H2SO4、⑫H2O反应,故路线为③→⑥→⑩→⑦→⑪→⑫,
故答案为:③→⑥→⑩→⑦→⑪→⑫;
(2)在能和盐酸反应的物质中,NaOH、Cu(OH)2和氨水为碱,化学方程式分别为:HCl+NaOH=NaCl+H2O、2HCl+Cu(OH)2=Cu(OH)2+2H2O、HCl+NH3•H2O=NH4Cl+H2O,
故答案为:HCl+NaOH=NaCl+H2O、2HCl+Cu(OH)2=Cu(OH)2+2H2O、HCl+NH3•H2O=NH4Cl+H2O;
(3)在水溶液中和熔融状态下均不能导电的化合物为非电解质,包括蔗糖、酒精、非金属氧化物和氨气等,故属于非电解质的是SO2,故答案为:⑩;
(4)CaCO3是强电解质,能完全电离为钙离子和碳酸根,故用等号,电离方程式为:CaCO3=Ca2++CO32-,故答案为:CaCO3=Ca2++CO32-;
(5)CaCO3是弱酸盐,能和盐酸发生复分解反应生成氯化钙和、二氧化碳,故离子方程式为:2H++CaCO3=Ca2++CO2↑+H2O,故答案为:2H++CaCO3=Ca2++CO2↑+H2O;
(6)一个化学方程式能拆出的Ag++Cl-=AgCl↓形式,说明是可溶性银盐和盐酸或可溶性盐酸盐反应,生成氯化银和一种强酸或可溶性盐,故对应的化学方程式可以为:AgNO3+NaCl=AgCl↓+NaNO3,故答案为:AgNO3+NaCl=AgCl↓+NaNO3.
点评 本题考查了电解质与非电解质的概念、常见元素单质及其化合物性质,题目难度不大,注意掌握电解质与非电解质的区别,(6)为易错点,注意题中信息要求.


科目:高中化学 来源: 题型:实验题
 某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液.检验其中OH-的实验方法省略,检验其他阴离子的过程如图所示.
某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液.检验其中OH-的实验方法省略,检验其他阴离子的过程如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
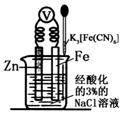
| A. | 该装置为电解池 | |
| B. | 本实验牺牲了金属Fe来保护金属Zn | |
| C. | 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀 | |
| D. | 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 一般不用纯碱代替小苏打作食品发酵粉 | |
| C. | 用甲醛溶液浸泡海产品以保鲜 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
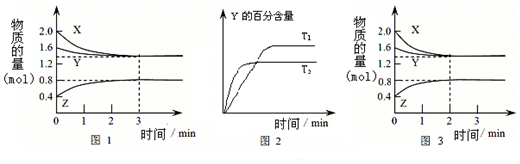
| A. | 容器中发生的反应可表示为:2X(g)+Y(g)?2Z(g) | |
| B. | 0~3 min内,v(X)=0.2 mol•L-1•min-1 | |
| C. | 其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 | |
| D. | 若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
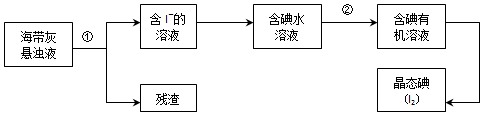
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.60 | 20.50 |
| 第二次 | 10.00 | 3.00 | 23.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com