
【题目】某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键或双键)。
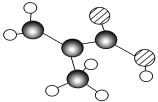
(1)该物质的结构简式为________。
(2)该物质中所含官能团的名称为___________________。
(3)下列物质中,与该产品互为同系物的是(填序号)________,互为同分异构体的是
________。
①CH3CH===CHCOOH ②CH2===CHCOOCH3
③CH3CH2CH===CHCOOH ④CH3CH(CH3)COOH
科目:高中化学 来源: 题型:
【题目】下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是
A.三种微粒所含有的电子数相等
B.三种微粒中氮原子的杂化方式相同
C.三种微粒的空间构型相同
D.键角大小关系:NH4+>NH3>NH2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学式为C2H6O的化合物A具有如下性质:A+Na―→慢慢产生气泡
A+CH3COOH![]() 有香味的产物
有香味的产物
(1)根据上述信息,对该化合物可作出的判断是( )。
A.一定含有—OH B.一定含有—COOH C.A为乙醇 D.A为乙醛
(2)含A的体积分数为75%的水溶液可以用作_______________________。
(3)A与钠反应的化学方程式:______________________________________________。
(4)化合物A与CH3COOH反应生成的有香味的产物的结构简式为:________。
(5)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式:___________________。
(6)如图是B分子的球棍模型和A分子的比例模型,若A和B的关系是同系物,则B的结构简式_____。
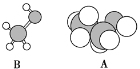
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是 。
(2)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水。为研究E的组成与结构,通过实验得到如下信息:
①有机物E的相对分子量为90。9.0g E完全燃烧时,生成CO2 0.3mol, H2O5.4g。则有机物E的分子式为 。
②实验证实其中含有羟基,羧基,甲基,则E的结构简式为 。
③写出E与足量Na的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
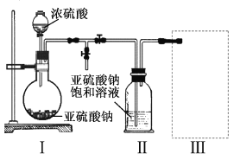
实验一焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置II中有Na2S2O5晶体析出,发生的反应为:
Na2SO3+SO2=Na2S2O5
(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是 。
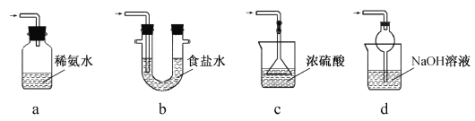
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 。(填序号)。
实验二焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)检验Na2S2O5晶体在空气中已被氧化的实验方案是 。
实验三葡萄酒中抗氧化剂残留量的测定
(5)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:馏分中的二氧化硫在滴入碘水时发生的反应为
SO2+I2+2H2O=H2SO4+2HI)在测定时消耗了0.01mol·L-1的I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:


(1)常温下含碳量最高的气态烃是________(填字母)。
(2)能够发生加成反应的烃有________种。
(3)一卤代物种类最多的是________(填写字母)。
(4)写出实验室制D的化学方程式:
_____________________________________________________________
(5)写出F发生硝化反应的化学方程式:
_____________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、硫、氯、砷等是农药中的重要组成元素。请回答下列问题:
(1)基态砷的价电子排布式是___________________________;
(2)氨气比PH3沸点高的原因是______________________;
(3)下列有关氮、磷、硫、氯的说法正确的是__________;
a.第一电离能由小到大的顺序是S<P<Cl
b.PO43-、SO42-、ClO4-互为等电子体,它们的空间构型均为四面体
c.磷、硫、氯基态原子的未成对电子数依次增多
d.1mol(C2H5O)P=0分子中含有的δ键的数目为24×6.02×1023
(4)氮化硼和磷化硼是受到高度关注的耐高温、耐磨涂料,两者结构相似。磷化硼晶胞结构如图所示,则磷化硼晶体中每个硼原子周围距离最近的磷原子数目为__________;晶体结构中存在的化学键有_______(填序号);

a.离子键b.共价键c.分子间作用力d.配位键
氮化硼晶体的熔点要比磷化硼晶体高,其原因______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com