
【题目】镁、铝、硫和钡元素是高中化学常见的元素,请运用相关性质回答下列问题:
(1)镁、钡是位于同一主族的活泼金属元素。钡在元素周期表中的位置是:_______。铝也是一种活泼金属,钡的金属性比铝的_______(填“强”或“弱”)。工业上可用如下方法制取钡:Al+BaO![]() Ba↑+BaO· Al2O3,该法制钡的主要原因是_________。BaO· Al2O3的物质种类是_______(填“酸、碱、盐或氧化物”等)。
Ba↑+BaO· Al2O3,该法制钡的主要原因是_________。BaO· Al2O3的物质种类是_______(填“酸、碱、盐或氧化物”等)。
(2) Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3固体配成溶液。
笫二步:加入适量H2SO4溶液和KI固体,滴加指示剂
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为VmL
则c(Na2S2O3)=______mol/L。(已知:2S2O32-+I2=S4O62-+2I-)
某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的Na2S2O3浓度可能_____(填“不受影响”、“偏低”或“偏高”),原因是 __________ (用离子方程式表示)。
【答案】 第六周期第IIA族 强 Ba的沸点比Al的低 盐 6000a/214V 或 3000a/107V 偏低 O2+4H++4I -=2I2+2H2O
【解析】(1)钡位于周期表第六周期,镁、钡是位于同一主族的金属元素,钡原子最外层电子的电子数为2,位于第六周期第IIA族;利用元素Ba、Al在元素周期表的位置可知金属活泼性:Ba>Al;Al在高温下可将氧化钡中钡置换出来,原因是Ba的沸点低于铝,高温时Ba转化为气体脱离反应体系,使反应正向进行,BaO· Al2O3是盐的氧化物表示形式,属于盐,故答案为:第六周期第IIA族;强;Ba的沸点比Al的低;盐;
(2)发生的反应有:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2Na2S2O3=Na2S4O6+2NaI;n(KIO3)= ![]() mol,设参加反应的Na2S2O3为xmol;
mol,设参加反应的Na2S2O3为xmol;
KIO3~~~~3I2~~~~6Na2S2O3
1 6
![]() mol xmol
mol xmol
所以 x=![]() ,则c(Na2S2O3)=
,则c(Na2S2O3)= ![]() =
= =
=![]() molL-1,第三步滴速太慢,I-被空气氧化,发生4I-+4H++O2═2I2+2H2O,消耗的Na2S2O3溶液的体积偏大,由c(Na2S2O3)=
molL-1,第三步滴速太慢,I-被空气氧化,发生4I-+4H++O2═2I2+2H2O,消耗的Na2S2O3溶液的体积偏大,由c(Na2S2O3)= ![]() molL-1,V偏大,c偏低,故答案为:
molL-1,V偏大,c偏低,故答案为: ![]() ;偏低;4I-+4H++O2═2I2+2H2O。
;偏低;4I-+4H++O2═2I2+2H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,酸性溶液A中可能含有NH4+、K+、Na+、Fe2+、Al3+、Fe3+、CO32-、NO3-、Cl-、I-、SO42-中的几种,现取该溶液进行有关实验,实验结果如下图所示:

回答下列问题:
(1)溶液A中一定存在的离子有___________________
(2)生成沉淀甲的离子方程式为___________________
(3)生成气体丙的离子方程式为__________________,若实验消耗Cu 144g,则最多生成气体丙的体积(标准状况下)为_____。
依据上述实验,某小组同学通过讨论后认为:溶液中可能含有的离子有NH4+、K+、Na+ 、Cl-、SO42-。为进一步确认溶液中存在的离子,分别取100ml废水又进行了如下图所示的三组实验:

(4)根据上述实验可进一步确定NH4+、K+、Na+ 、Cl-、SO42-中一定存在的离子有 _________ ,沉淀溶解时发生反应的离子方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( ) 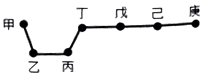
A.甲一定是金属元素
B.气态氢化物的稳定性:庚>己>戊
C.乙、丙、丁的最高价氧化物水化物可以以相互反应
D.庚的最高价氧化物水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯只有 ![]() 和
和 ![]() 两各稳定同位素,它们在氯气中的原子数之比
两各稳定同位素,它们在氯气中的原子数之比 ![]() :
: ![]() 为3:1.则相对分子质量为70、72、74、的氯气分子数之比可能是( )
为3:1.则相对分子质量为70、72、74、的氯气分子数之比可能是( )
A.5:2:1
B.5:2:2
C.9:3:1
D.9:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国每年产生的废旧铅蓄电池约330万吨,从含铅废料(PbSO4、PbO2、PbO等)中回收铅,实现铅的再生,意义重大。一种回收铅的工作流程如下:

(1)铅蓄电池放电时,PbO2作_______极。
(2)过程 I ,己知:PbSO4、PbCO3 的溶解度(20℃)见图 1; Na2SO4、Na2CO3的 溶解度见图2。

①根据图1写出过程I的离子方程式:_____________。
②生产过程中的温度应保持在40℃。若温度降低,PbSO4的转化速率下降。根据图2,解释原因:
i.温度降低,反应速率降低;
ii._______________(请你提出一种合理解释)。
(3)过程 II,发生反应 2PbO2 + H2C2O4=2PbO + H2O2 + 2CO2↑。PbO与 Al2O3性质相似,PbO与氢氧化钠溶液反应的离子方程式是________________。
(4)过程Ⅲ,将PbO粗品溶解在H2SO4和NaCl的混合溶液中,得到含Na2PbCl4的电解液。电解Na2PbCl4溶液,生成Pb,如下图。

①阴极的电极反应式是____________。
②电解一段时间后,Na2PbCl4浓度极大下降,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某蛋白质分子有A、B两条肽链,A链有31个氨基酸,B链有42个氨基酸。该蛋白质分子中肽键的数目是 ( )
A. 70个 B. 71个 C. 72个 D. 73个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017北京]下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com