
���ۺ�ͭ�۵ľ��Ȼ���ƽ���ֳ��ĵȷݣ��ֱ����ͬŨ�ȵ�ϡ���ᣬ��ַ�Ӧ���ڱ�״��������NO�������ʣ��������������±���������Ļ�ԭ����ֻ��NO����
| ��� | �� | �� | �� | �� |
| ϡ�������/mL | 100 | 200 | 300 | 400 |
| ʣ�����/g | 18.0 | 9.6 | 0 | 0 |
| NO���/mL | 2240 | 4480 | 6720 | V |
��ش��������⣺
��1����ԭ������У���μ���������ᣬ��ַ�Ӧ������˵����ȷ���� ��
a. �����ȷ�Ӧ������Fe2+
b. ����ȫ���ܽ��ͭ�۲ŷ�Ӧ
c. �����Һ�к�Fe3+��Cu2+
��2����ʵ���У����������Ũ��Ϊ ��
��3����ʵ����У��ܽ���Fe�������Ƿ�Ϊ5.6g�� ��ʵ������ܽ���Cu�Ƿ�Ϊ9.6g�� ����ǡ�����
��4����ʵ����У�V��ֵΪ�� ��
��1��abc ��2��4.00mol/L�� ��3���� �� ��4��8960mL
������
��2����ʵ������н���ʣ���֪����Ӧ���н�������+2�ۡ���ݷ���ʽ��
3M+8HNO3��ϡ��===3M��NO3��2+2NO��+4H2O �ٵ�
![]()
��3����ʵ�����ʵ��ٵ����ݷ�����ƽ��ÿʧ1mol�����ܽ�Ľ���������Ϊ��
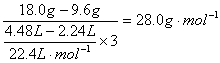
�ɴ˿��ж��ܽ�Ľ���������
ʵ�����ת�Ƶĵ���Ϊ
![]()
��ʵ��3��ʵ��2�����ݷ�����ƽ��ÿʧ1mol������Һ�Ľ���������Ϊ��
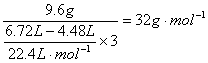
�ɴ˿��жϸ�9.6g������ͭ��
��4��ÿ�ݽ��������Ϊ![]() ��
��![]() ��
��
������400mLϡ����ʱ������ȫ����������ʵ��۵Ļ����ϣ�Fe2+��ʧ���ӣ�
![]() ��ϡ�����ٱ���ԭ����NO��
��ϡ�����ٱ���ԭ����NO��
![]() �����ԣ�ʵ��4����������
�����ԣ�ʵ��4����������
![]()


 ��������ϵ�д�
��������ϵ�д� ����˼ά����ѵ����ʱ��ѧ��ϵ�д�
����˼ά����ѵ����ʱ��ѧ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������������ ���ͣ�038
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�038
���ۺ�ͭ�۹�14.8g����������ۻ�Ͼ��ȣ�����ʹ֮��ȫ��Ӧ���õ�21.2g��ɫ���壬��ԭ������ĩ�����۵�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2009-2010ѧ��㶫ʡտ�����и������ϣ��ڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com