
【题目】人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农生产及日常生活方面用途非常广泛。试回答下列问题。
(1)Cu+的核外电子排布式为___________________________________;
(2)铜镁合金是一种储氢材料,某种铜镁互化物晶胞结构如图,则该互化物的化学式为___________;

(3)叠氮化铜[Cu(N3)2]是一种紫黑色粉末,易爆炸,与N3-互为等电子体的分子有___________(举2例).
(4)丁炔铜是一种优良的催化剂,已知:CH≡CH+2HCHO![]() OHC-CH2CH2OH;
OHC-CH2CH2OH;
OHC-CH2CH2OH中碳原子杂化方式有___________,乙炔属于___________(填“极性”或“非极性”)分子.
(5)若向盛有CuSO4溶液的试管里加入氨水,首先形成蓝色难溶物,继续加入氨水,难溶物溶解,变成蓝色透明溶液,这时得到一种称溶质的化学式为___________,其中含有的化学键类型有______________________;
(6)已知铜镁互化物晶胞参数为apm,则该晶胞的密度为_______________。
【答案】(1)[Ar]3d10或1s22s22p63s23p63d10(2) MgCu2 (3)CO2、N2O (4) sp2、sp3 非极性(5)[Cu(NH3)4]SO4 离子键、共价键(极性键)、配位键 (6)![]() g/cm3
g/cm3
【解析】
试题分析:(1)铜为29号元素,根据原子核外电子排布规律可以写出Cu+的核外电子排布式为1s22s22p63s23p63d10;
(2)根据铜镁互化物晶胞结构,利用均摊法可知,在晶胞中含有铜原子数为8,镁原子数为8×+6×=4,所以铜原子与镁原子数目之比为2:1,据此写出化学式为MgCu2;
(3)N3-中有价电子数为16,三个原子,根据等电子体的概念可知,与N3-互为等电子体的分子有CO2、N2O等;
(4)OHC-CH2CH2OH中两种碳,一种是醛基中的碳,含C=O键,还有一种碳都以单键与其它原子相连,所以碳原子杂化方式有两种,即sp2、sp3,乙炔是直线型对称的分子,所以是非极性分子;
(5)根据名称硫酸四氨合铜,可以写出化学式为:[Cu(NH3)4]SO4,在硫酸四氨合铜中,N、H原子之间以共价键结合,Cu2+提供空轨道,N原子提供孤对电子,则以配位键结合,而硫酸根离子与四氨合铜配离子之间是离子键;
(6)铜镁互化物晶胞中含有4个MgCu2,参数为apm=a×10-9cm,晶胞的体积为a3×10-27cm3,则该晶胞的密度为![]() =
=![]() g/cm3。
g/cm3。


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】在研究合成氨方法的历史上,不同的研究者曾3次获诺贝尔化学奖。合成氨大大提高了农作物的产量,同时也是制取硝酸、炸药等的原料。下列说法中正确的是
A.N2和H2在点燃或光照条件下可合成氨气
B.氨和HNO3都是电解质
C.氨气遇到浓硝酸会发生反应产生大量白烟
D.由NH3制HNO3的过程中,氮元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017 年诺贝尔生理学或医学奖授予3位美国科学家Jffrey C. Hall, Michael Rosbash 和Michael w. Young以表彰他们发现了调控"生物钟”的分子机制。褪黑素(C13H16N2O2)是一种生物钟调节剂。请问褪黑素属于
A.氧化物B.无机物C.有机物D.烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝-空气-海水为能源的电池为我国首创,该电池用于航海标志灯,只要把灯放入海水中数秒钟,就会发出耀眼的白光。电极材料为Al与石墨。该电池工作时,下列说法正确的是
A.铝电极是该电池的正极B.海水中Cl-向石墨电极移动
C.石墨电极的反应:O2+2H2O+4e-=4OH-D.该新型电池属于二次电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一位厨师不小心把刚熬好的羊油碰翻在灶坑旁,与草木灰混在一起,当他将羊油与草木灰的混合物用手捧出去后,洗手时发现手洗得特别干净。对此下列解释正确的是
A.羊油是一种有机溶剂,溶解了厨师手上的油污
B.草木灰呈碱性,与羊油发生了中和反应,除去油污
C.羊油与草木灰中的物质发生了加成反应,除去油污
D.羊油在碱性草木灰(主要成分为K2CO3)的作用下发生了皂化反应,生成具有去油污能力的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面是我们熟悉的物质:
①O2 ②SO2 ③CaCl2 ④HNO3 ⑤NaOH ⑥NH4Cl
这些物质中,属于共价化合物的是 ___________;属于离子化合物的是___________;只含离子键的是___________。
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。

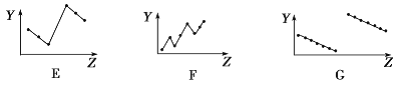
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数________________。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径________________。
③第二、三周期主族元素随原子序数递增原子半径的变化____________。
(3)已知某单核粒子的结构示意图为:![]()
①当x-y=10时,该粒子为____________(填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_____。
(4)已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系。

请写出:A的化学式 (写一种); D的化学式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。

步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收。2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水。
步骤二:通过仪器分析得知X的相对分子质量为106。
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3。如图Ⅰ。


步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ。
试填空:
(1)X的分子式为________;X的名称为 。
(2)步骤二中的仪器分析方法称为________。
(3)写出X与足量浓硝酸和浓硫酸混合物反应的化学方程式: 。
(4)写出X符合下列条件的同分异构体结构简式 。
①芳香烃 ②苯环上一氯代物有三种
(5)X以醋酸为溶剂在催化剂作用下用氧气氧化得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:25 ℃时0.25 g、50 ℃时0.97 g、95 ℃时7.17 g。得到的粗产品中有部分不溶性杂质,请简述实验室中提纯PTA的实验方案: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喷泉实验是一种常见的自然现象,其产生原因是存在压强差。在上图右图中的锥形 瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )

A. Cu与稀盐酸 B. NaHCO3与NaOH溶液
C. CaCO3与稀硫酸 D. NH4HCO3与稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿石含碳酸镁和石英,制备高纯硅和硅胶的工艺流程如下:

(1)“硅胶”冶常用作_______________ ,也可以用作__________的载体。 A 的结构式为________。
(2)制备粗硅的方程式为_______。
(3)操作I为_____________,操作Ⅱ为_______________,操作Ⅲ所用仪器有铁架台(带铁圈)、酒精灯、_______________等。
(4)操作Ⅲ,需要在氯化氢气流中加热脱水的原因是_______________。
(5)溶液G用E酸化的方程式为_______________。
(6)电解饱和的K溶液的离子方程式为____________,阳极电极方程式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com