
【题目】有铁和锌的混合物共9.3g,与500mL盐酸恰好完全反应,在标准状况下共收集到3.36LH2 , 求:
(1)铁的质量是g;
(2)反应前,盐酸的物质的量浓度为mol/L;
(3)写出锌与盐酸反应的离子方程式并用双线桥表示电子转移.
【答案】
(1)2.8
(2)0.6
(3)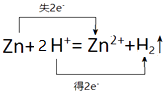
【解析】解:(1)令铁和锌的物质的量分别为amol、bmol,则:
Fe~~ | H2 | Zn~~ | H2 |
amol | amol | bmol | bmol |
所以 ![]()
解得:a=0.05,b=0.1
故混合物铁的质量为0.05mol×56g/mol=2.8g,
所以答案是:2.8;
(2)标准状况下3.36L H2的物质的量为 ![]() =0.15mol,所以根据H元素守恒,则HCl的物质的量为0.15mol×2=0.3mol,所以c=
=0.15mol,所以根据H元素守恒,则HCl的物质的量为0.15mol×2=0.3mol,所以c= ![]() =
= ![]() =0.6mol/L;
=0.6mol/L;
所以答案是:0.6;
(3)锌与盐酸反应生成锌离子和氢气,其中锌失电子,氢离子得电子,转移电子数为2e﹣,所以用双线桥表示电子转移为:
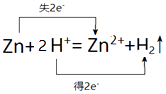 ,
,
所以答案是: 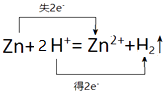 .
.


科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近.在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究. 
(1)仪器D的名称是 , 安装F中导管时,应选用图2中的 .
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2 , 此时F中溶液的颜色不变,则装置C的作用是 .
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 该反应的离子方程式为 , 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 .
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是 , 原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物中,在铜的作用下催化氧化,又能发生消去反应,且消去生成物中存在同分异构体的是( )
A.CH3 CH2C(OH)(CH3)2
B.(CH3)2CHOH
C.CH3CH(OH)CH2 CH3
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素的原子序数,可以推知原子的①质子数②核电荷数③核外电子数④在周期表中的位置,其中正确的是( )
A. ①③④B. ②③④C. ①②③D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某饱和一氯代烷3.70g与足量的NaOH水溶液混合加热后,用HNO3酸化,再加入足量AgNO3溶液,生成白色沉淀5.74g.则该卤代烃的分子式为: , 这种一氯代物的同分异构体种类有种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乙烯和苯都能发生加成反应
B.乙醇和乙酸都能与氢氧化钠溶液反应
C.淀粉和蛋白质水解产物都是氨基酸
D.葡萄糖和蔗糖都可发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的水溶液显酸性,遇FeCl3溶液不显色,A分子结构中不含甲基,含苯环,苯环上的一氯代物只有两种,A和其他有机物存在如下图所示的转化关系: 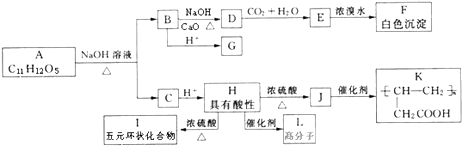
已知: ![]() +NaOH
+NaOH ![]() R﹣H+Na2CO3
R﹣H+Na2CO3
试回答下列问题:
(1)B化学式 .
(2)H→I反应类型为 , J所含官能团的名称为 .
(3)写出H→L 反应的化学方程式 .
(4)A的结构简式;A生成B和C的反应方程式: .
(5)F的同分异构体中含有苯环且官能团相同的物质共有种(不包括F),其中核磁共振氢谱有两个峰,且峰面积比为1:2的是(写结构简式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ag/A12O3催化剂在工业上具有广泛用途.废银催化剂中银的回收既可节约资源,又有较好的经济效益.回收银的简化流程如图所示(部分条件和试剂略): 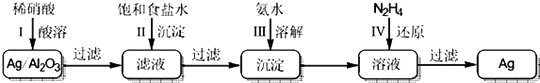
请回答下列问题:
(1)第Ⅰ步中,载体A12O3不与稀硝酸反应.Ag和稀硝酸反应产生的气体是
(2)第Ⅱ步中,饱和食盐水由工业食盐水提纯而得.除去工业食盐水中的少量Na2SO4、MgC12、CaC12杂质,正确的操作顺序是(填字母编号).
a.加入稍过量的NaOH溶液 b.加入稍过量的BaC12溶液 c.过滤
d.加入稍过量的Na2CO3溶液 e.加入适量盐酸
(3)第III步中,加入氨水使沉淀溶解的离子方程式是
(4)N2H4具有还原性,氧化产物为N2 . 第IV步反应的产物除Ag和N2外,还有的物质是(填化学式).
(5)N2H4可用作火箭推进剂.已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJ/mol
2NO(g)+O2(g)=2NO2(g)△H=﹣116kJ/mol
N2(g)+O2(g)=2NO(g)△H=+183kJ/mol
N2H4和NO2反应生成N2和气态H2O的热化学方程式是 .
(6)Ag可制备银锌纽扣电池正极材料Ag2O2 , 碱性条件下该电池的正极反应式是 .
(7)若上述流程中第Ⅰ、Ⅱ、Ⅲ步银的回收率均为90%,则处理以a kg含银b%的废银催化剂,理论上需要加入N2H4的质量是kg.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com