
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | ______ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
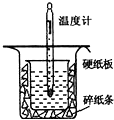
| 3.4℃+3.3℃+3.5℃, |
| 3 |
| 1.421kJ |
| 0.025mol |


科目:高中化学 来源:不详 题型:单选题
| A.通过品红溶液 |
| B.通过澄清石灰水 |
| C.先通过NaOH溶液,再通过澄清石灰水 |
| D.先通过酸性KMnO4,再通过澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④③①⑤② | B.④②③⑤① | C.①⑤③④② | D.③④①⑤② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用铂丝蘸取氯化钠溶液灼烧,可看到火焰呈紫色 |
| B.在稀硫酸溶液中滴加氯化钡溶液,会产生白色沉淀 |
| C.二氧化硫通入品红溶液中能使品红溶液褪色 |
| D.向紫色石蕊试液中滴加氯水,溶液颜色先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
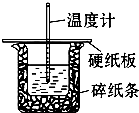
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
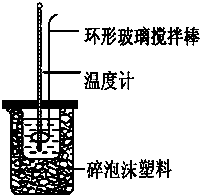
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
| 1 | 20.00 | 11.95 |
| 2 | 20.00 | 13.00 |
| 3 | 20.00 | 12.05 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.前者产生的氯气多 | B.一样多 |
| C.后者产生的氯气多 | D.无法比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com