
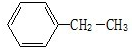
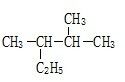
 :苯环连接乙基,是苯的同系物,该有机物命名为:乙苯,
:苯环连接乙基,是苯的同系物,该有机物命名为:乙苯,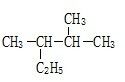 是烷烃,选取含有最多碳原子的碳链为主链,主链含有5个C,为戊烷,从离甲基最近的一端编号,该有机物命名为:2,3-二甲基戊烷,
是烷烃,选取含有最多碳原子的碳链为主链,主链含有5个C,为戊烷,从离甲基最近的一端编号,该有机物命名为:2,3-二甲基戊烷, ,
, ;
;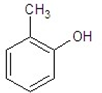 ,
, ;
;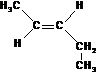 ,
,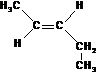 .
.


科目:高中化学 来源: 题型:
| A、在c(H+)=1.0×10-13mol?L-1的溶液中:Na+、S2-、AlO2-、SO32- | ||||
| B、含有0.1 mol?L-1 Fe2+的溶液:Na+、ClO-、SO42-、Cl- | ||||
C、含有0.1 mol?L-1HCO
| ||||
D、强酸性溶液:K+、Al3+、NO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
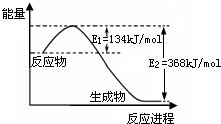 氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.| 催化剂 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
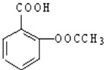 ,难溶于水.为了使疗效更好,它可与
,难溶于水.为了使疗效更好,它可与查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22g乙醛中含有σ键3NA |
| B、1.0L 0.1mol/L Na2S溶液中阴离子总数小于0.1NA |
| C、对于Si+O2=SiO2,每当形成2NA个Si-O键,需断开NA个Si-Si键 |
| D、某核素Cl的质量数为a,其摩尔质量为aNA g/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com